Cos'è Briladona?
Briladona è un farmaco a base del principio attivo Norgestimato + Etinilestradiolo , appartenente alla categoria degli Contraccettivi ormonali sistemici e nello specifico Associazioni fisse estro-progestiniche. E' commercializzato in Italia dall'azienda Exeltis Italia S.r.l. .
Briladona può essere prescritto con RicettaRR - medicinali soggetti a prescrizione medica .
Briladona può essere prescritto con Ricetta
Confezioni
Briladona 0,25 mg/0,035 mg 21 compresse
Briladona 0,25 mg/0,035 mg 63 compresse
Briladona 0,25 mg/0,035 mg 63 compresse
Informazioni commerciali sulla prescrizione
Titolare: Exeltis Healthcare S.L.
Concessionario:Exeltis Italia S.r.l.
Ricetta:RR - medicinali soggetti a prescrizione medica
Classe:C
Principio attivo:Norgestimato + Etinilestradiolo
Gruppo terapeutico:Contraccettivi ormonali sistemici
ATC:G03AA11 - Norgestimato ed etinilestradiolo
Forma farmaceutica: compressa
Concessionario:
Ricetta:
Classe:
Principio attivo:
Gruppo terapeutico:
ATC:
Forma farmaceutica: compressa
Se sei un professionista, potrai trovare le schede tecniche complete e molto altro nell'area riservata di Codifa.it
Indicazioni
Perché si usa Briladona? A cosa serve?
Contraccezione orale
La decisione di prescrivere Briladona deve prendere in considerazione i fattori di rischio attuali della singola donna, in particolare quelli relativi alle tromboembolie venose (TEV) e il confronto tra il rischio di TEV associato a Briladona e quello associato ad altri contraccettivi ormonali combinati (COC) (vedere paragrafi 4.3 e 4.4).
Posologia
Come usare Briladona: Posologia
Per somministrazione orale.
Come usare le compresse di Briladona
Le compresse devono essere assunte ogni giorno approssimativamente alla stessa ora, se necessario con un po' di liquido, nell'ordine indicato sul blister. Si deve assumere una compressa al giorno per 21 giorni consecutivi. Ogni blister successivo deve essere iniziato dopo un intervallo di 7 giorni senza compresse, durante il quale ha luogo di solito un'emorragia da interruzione. Ciò inizia di solito al 2°-3° giorno dopo l'assunzione dell'ultima compressa e può non essere terminata prima che si inizi il blister successivo.
Come iniziare Briladona
- Nessun uso di contraccettivi ormonali (nel mese precedente)
L'assunzione deve iniziare il primo giorno del ciclo naturale (cioè il primo giorno di mestruazione).
È possibile iniziare fra il 2° e il 5° giorno, ma in questo caso si consiglia di utilizzare in aggiunta un metodo barriera durante i primi 7 giorni del primo ciclo di assunzione. - Passaggio da un metodo contraccettivo ormonale combinato (contraccettivo orale combinato , anello vaginale o cerotto transdermico)
La donna deve iniziare l'assunzione di Briladona preferibilmente il giorno dopo l'assunzione dell'ultima compressa attiva (l'ultima compressa contenente i principi attivi) del contraccettivo orale combinato precedente, ma al più tardi il giorno dopo il consueto intervallo senza compressa o il giorno dopo l'ultima compressa placebo del contraccettivo orale combinato precedente. Nel caso siano stati utilizzati anello vaginale o cerotto transdermico, la donna deve iniziare l'assunzione di Briladona preferibilmente il giorno della rimozione, ma al più tardi quando sarebbe dovuta iniziare l'applicazione successiva.
Passaggio da un metodo a base di solo progestinico (pillola a base di solo progestinico, forme iniettabili, impianti) o da un dispositivo intrauterino che rilascia progestinico (IUD)
La donna può effettuare il passaggio a Briladona in qualsiasi giorno dalla pillola a base di solo progestinico (da un impianto o da un IUD dal giorno della rimozione, da una forma iniettabile da quando sarebbe dovuta avvenire la successiva iniezione) ma, in ognuno di questi casi, deve essere informata di utilizzare in aggiunta un metodo barriera durante i primi 7 giorni di assunzione delle compresse. - Dopo un aborto avvenuto al primo trimestre
La donna può iniziare l'assunzione immediatamente. In questo caso, non è richiesta alcuna misura contraccettiva aggiuntiva. - Dopo un parto o dopo un aborto avvenuto nel secondo trimestre
Le donne devono essere informate di iniziare dal giorno 21 al giorno 28 dopo il parto o dopo l'aborto avvenuto nel secondo trimestre. Se si inizia più tardi, la donna deve essere informata di usare un metodo barriera aggiuntivo per i primi 7 giorni di assunzione delle compresse. Tuttavia, se c'è già stato un rapporto sessuale, si deve escludere la possibilità di una gravidanza prima di iniziare l'assunzione di un contraccettivo orale combinato o la donna deve attendere fino al suo primo ciclo mestruale.
Per le donne che allattano al seno vedere il paragrafo 4.6.
Gestione delle compresse dimenticate
Se l'utilizzatrice ha un ritardo inferiore a 12 ore nell'assunzione della compressa, l'efficacia contraccettiva non è compromessa. La donna deve assumere la compressa non appena lo ricorda e deve assumere le compresse successive alla solita ora.
Se la donna ha un ritardo superiore a 12 ore nell'assunzione della compressa, la protezione contraccettiva può essere ridotta.
La gestione delle compresse dimenticate può essere guidata dalle seguenti due regole di base:
- L'assunzione delle compresse non deve mai essere interrotta per più di 7 giorni.
- Per ottenere un'adeguata soppressione dell'asse ipotalamo-ipofisi-ovaio sono necessari 7 giorni di assunzione ininterrotta delle compresse.
Di conseguenza, si possono dare i seguenti consigli per la pratica quotidiana:
Giorno 1-7
La donna deve assumere l'ultima compressa dimenticata appena se ne ricorda, anche se ciò significa assumere due compresse contemporaneamente. La donna continua poi assumendo le compresse all'ora consueta. In aggiunta, deve essere utilizzato un metodo barriera, come il profilattico, per i 7 giorni successivi. Se c'è stato un rapporto sessuale nei 7 giorni precedenti, si deve prendere in considerazione la possibilità di una gravidanza. Quanto maggiore è il numero di compresse dimenticate e quanto più tale dimenticanza è vicina all'intervallo senza compresse, tanto più elevato sarà il rischio di una gravidanza.
Giorno 8-14
La donna deve assumere l'ultima compressa dimenticata appena se ne ricorda, anche se ciò significa assumere due compresse contemporaneamente. La donna continua poi assumendo le compresse all'ora consueta. Se la donna ha assunto le compresse correttamente nei 7 giorni precedenti la prima compressa dimenticata, non è necessario utilizzare altre precauzioni contraccettive. Tuttavia, se ha dimenticato più di una compressa, la donna deve essere avvisata di prendere precauzioni aggiuntive per 7 giorni.
Giorno 15-21
Il rischio che l'affidabilità sia ridotta è imminente in quanto si avvicina l'intervallo di 7 giorni senza compresse. Tuttavia, modificando l'assunzione delle compresse, è ancora possibile impedire la riduzione della protezione contraccettiva. Aderendo ad una delle seguenti due opzioni, non è pertanto necessario usare precauzioni contraccettive aggiuntive, a condizione che nei 7 giorni precedenti la prima compressa dimenticata la donna abbia assunto correttamente tutte le compresse. In caso contrario, la donna deve seguire la prima di queste due opzioni e usare anche precauzioni aggiuntive per i successivi 7 giorni.
- La donna deve prendere l'ultima compressa dimenticata non appena se ne ricorda, anche se questo significa prendere due compresse contemporaneamente. La donna continua poi assumendo le compresse all'ora consueta. Il blister successivo deve essere iniziato appena viene terminato il blister in uso, cioè non si deve lasciare l'intervallo fra i blister. È improbabile che la donna abbia un'emorragia da sospensione fino al termine delle compresse del secondo blister, ma potrebbero verificarsi macchie di sangue (spotting) o sanguinamento da interruzione nei giorni di assunzione delle compresse.
- La donna deve essere anche informata di sospendere l'assunzione delle compresse dal blister in uso. Deve avere un intervallo senza compresse fino a 7 giorni, inclusi i giorni in cui ha dimenticato le compresse, e in seguito continuare con il successivo blister.
Se la donna ha dimenticato delle compresse e successivamente non si presenta un'emorragia da sospensione nel primo normale intervallo senza compresse, deve essere considerata l'eventualità di una gravidanza.
Come ritardare l'emorragia da interruzione
Per ritardare le mestruazioni, la donna deve continuare con un altro blister di Briladona senza l'intervallo libero da compresse. Il ritardo può essere protratto per quanto tempo si desidera, fino al termine delle compresse attive nel secondo blister. In questo periodo di estensione, la donna può manifestare metrorragia da interruzione o macchie di sangue (spotting). La regolare assunzione di Briladona viene quindi ripresa dopo la fase di intervallo senza compresse.
Se la donna vuole spostare il giorno di inizio delle mestruazioni a un altro giorno della settimana, deve essere consigliata di accorciare il periodo senza compresse di quanti giorni desidera. Più breve è l'intervallo, maggiore è il rischio che non si presenti un'emorragia da interruzione e che si presentino invece metrorragia da interruzione e macchie di sangue (spotting) durante la confezione successiva (come quando si ritardano le mestruazioni).
Consigli in caso di disturbi gastrointestinali
In caso di gravi disturbi gastro-intestinali (per esempio vomito o diarrea ), l'assorbimento del principio attivo può non essere completo e devono essere prese misure contraccettive aggiuntive.
Se si verifica vomito o diarrea grave entro 3-4 ore dopo l'assunzione della compressa attiva, deve essere assunta una nuova compressa (in sostituzione) appena possibile. La nuova compressa deve essere assunta entro 12 ore dall'ora abituale di assunzione, se possibile. Se sono trascorse più di 12 ore, si applicano i consigli sulle compresse dimenticate, forniti al paragrafo 4.2 “Gestione delle compresse dimenticate”. Se la donna non vuole modificare l'abituale schema di assunzione delle compresse, deve prendere la(e) compressa(e) aggiuntiva(e) da un altro blister.
Anziani
L'uso di questo prodotto non è indicato nelle donne in post-menopausa.
Bambine
L'uso di questo prodotto non è indicato prima del menarca.
Controindicazioni
Quando non dev'essere usato Briladona
- Presenza o rischio di tromboembolia venosa (TEV)
- Tromboembolia venosa - TEV in corso (con assunzione di anticoagulanti) o pregressa (per es. trombosi venosa profonda [TVP] o embolia polmonare [EP])
- Predisposizione ereditaria o acquisita nota alla tromboembolia venosa, come resistenza alla proteina C attivata (incluso fattore V di Leiden), carenza di antitrombina III, carenza di proteina C, carenza di proteina S (vedere paragrafo 4.4)
- Intervento chirurgico maggiore con immobilizzazione prolungata (vedere paragrafo 4.4)
- Rischio elevato di tromboembolia venosa dovuto alla presenza di più fattori di rischio (vedere paragrafo 4.4)
- Presenza o rischio di tromboembolia arteriosa (TEA
- Tromboembolia arteriosa – tromboembolia arteriosa in corso o pregressa (ad es. infarto miocardico) o condizioni prodromiche (ad es. angina pectoris)
- Malattia cerebrovascolare – ictus in corso o pregresso o condizioni prodromiche (ad es. attacco ischemico transitorio, TIA)
- Predisposizione ereditaria o acquisita nota alla tromboembolia arteriosa, come iperomocisteinemia e anticorpi antifosfolipidi (anticorpi anticardiolipina, lupus anticoagulante).
- Precedenti di emicrania con sintomi neurologici focali.
- Rischio elevato di tromboembolia arteriosa dovuto alla presenza di più fattori di rischio (vedere paragrafo 4.4) o alla presenza di un fattore di rischio grave come:
- diabete mellito con sintomi vascolari
- ipertensione grave
- dislipoproteinemia grave
- Patologia del fegato grave in atto o pregressa, fino a quando i valori di funzionalità epatica non sono tornati alla normalità
- Tumore epatico in atto o pregresso (benigno o maligno)
- Condizioni maligne note o sospette degli organi genitali o delle mammelle) se influenzate da steroidi sessuali
- Iperplasia dell'endometrio
- Sanguinamento vaginale di natura non accertata
- Ittero colestatico della gravidanza o ittero con uso precedente della pillola
- Malattia cardiaca valvolare con complicanze
- Pancreatite o pancreatite pregressa se associata a ipertrigliceridemia grave
- Ipersensibilità ai principi attivi o ad uno qualsiasi degli eccipienti elencati al paragrafo 6.1
È controindicato l'uso contemporaneo di Briladona con medicinali contenenti ombitasvir/paritaprevir/ ritonavir e dasabuvir, medicinali contenenti glecaprevir/pibrentasvir o sofosbuvir/velpatasvir/voxilaprevir (vedere paragrafo 4.5).
Se una di queste condizioni si verifica per la prima volta durante l'uso di Briladona, le compresse devono essere immediatamente sospese.
Avvertenze speciali e precauzioni di impiego
Cosa serve sapere prima di prendere Briladona
Avvertenze
Nel caso in cui fosse presente una delle condizioni o uno dei fattori di rischio menzionati sotto, l'idoneità di Briladona deve essere discussa con la donna.
In caso di peggioramento o di prima comparsa di uno qualsiasi di questi fattori di rischio o di queste condizioni, la donna deve essere avvisata di rivolgersi al proprio medico per determinare se l'uso di Briladona debba essere interrotto.
Esami medici /visite mediche
Prima di iniziare o riprendere l'uso di Briladona, deve essere raccolta un'anamnesi completa (inclusa l'anamnesi familiare) e la gravidanza deve essere esclusa. Deve essere misurata la pressione arteriosa e deve essere eseguito un esame clinico, guidato dalle controindicazioni (vedere paragrafo 4.3) e dalle avvertenze (vedere paragrafo 4.4).
È importante attirare l'attenzione della donna sulle informazioni relative alla trombosi venosa e arteriosa, incluso il rischio associato a Briladona rispetto ad altri COC, i sintomi di TEV e TEA, i fattori di rischio noti e cosa fare in caso di sospetta trombosi.
La donna deve anche essere informata della necessità di leggere attentamente il foglio illustrativo e di seguirne i consigli. La frequenza e il tipo di esami devono basarsi sulle linee guida stabilite e devono adattarsi alla singola donna.
Le donne devono essere informate che i contraccettivi orali non proteggono dalle infezioni da HIV (AIDS) e da altre malattie sessualmente trasmesse.
Disturbi circolatori
Rischio di tromboembolia venosa (TEV)
L'uso di qualsiasi contraccettivo ormonale combinato (COC) determina un aumento del rischio di tromboembolia venosa (TEV) rispetto al non uso. I prodotti che contengono levonorgestrel, norgestimato (compreso Briladona) o noretisterone sono associati a un rischio inferiore di TEV. La decisione di usare Briladona deve essere presa solo dopo aver discusso con la donna per assicurarsi che essa comprenda il rischio di TEV con Briladona, il modo in cui i suoi attuali fattori di rischio influenzano tale rischio e il fatto che il rischio che sviluppi una TEV è più alto nel primo anno di utilizzo. Vi sono anche alcune evidenze che il rischio aumenti quando l'assunzione di un COC viene ripresa dopo una pausa di 4 o più settimane.
Circa 2 donne su 10.000 che non usano un COC e che non sono in gravidanza svilupperanno una TEV nell'arco di un anno. In una singola donna, però, il rischio può essere molto superiore, a seconda dei suoi fattori di rischio sottostanti (vedere di seguito).
Si stima che su 10.000 donne che usano un COC contenente levonorgestrel, circa 6 donne svilupperanno una TEV in un anno.
Le attuali evidenze suggeriscono che il rischio di TEV con COC contenenti norgestimato è simile al rischio dei COC contenenti levonorgestrel.
Questo numero di TEV per anno è inferiore al numero previsto in gravidanza o nel periodo post-partum.
La TEV può essere fatale nell'1-2% dei casi.
Numero di eventi di TEV per 10.000 donne in un anno
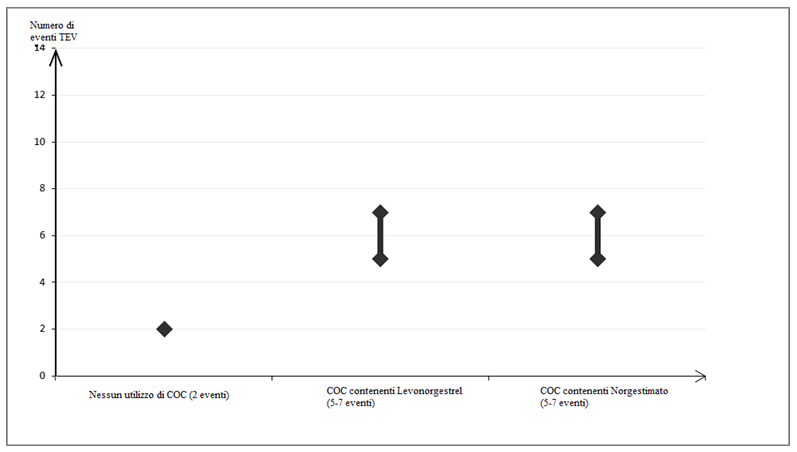
Molto raramente in donne che usano COC sono stati riportati casi di trombosi in altri vasi sanguigni, ad esempio vene e arterie epatiche, mesenteriche, renali, cerebrali o retiniche.
Fattori di rischio di TEV
Il rischio di complicanze tromboemboliche venose nelle donne che usano COC può aumentare notevolmente se sono presenti fattori di rischio aggiuntivi, specialmente se tali fattori di rischio sono più di uno (vedere la tabella).
Briladona è controindicato se una donna presenta diversi fattori di rischio che la pongono ad alto rischio di trombosi venosa (vedere paragrafo 4.3). Se una donna presenta più di un fattore di rischio, è possibile che l'aumento del rischio sia maggiore della somma dei singoli fattori; in questo caso deve essere considerato il suo rischio totale di TEV. Se si ritiene che il rapporto beneficio/rischio sia negativo, non si deve prescrivere un COC (vedere paragrafo 4.3).
Fattori di rischio di TEV
|
Fattore di rischio
|
Commento
|
|
Obesità (indice di massa corporea (IMC) superiore a 30 kg/m2)
|
Il rischio aumenta considerevolmente all'aumentare dell'IMC.
Particolarmente importante da considerare se sono presenti anche altri fattori di rischio.
|
|
Immobilizzazione prolungata, interventi chirurgici maggiori, interventi chirurgici di qualsiasi tipo a gambe e pelvi, interventi neurochirurgici o trauma maggiore
Nota: l'immobilizzazione temporanea, inclusi i viaggi in aereo di durata >4 ore, può anche essere un fattore di rischio di TEV, specialmente in donne con altri fattori di rischio
|
In queste situazioni è consigliabile interrompere l'uso della pillola (in caso di interventi elettivi almeno quattro settimane prima) e non riavviarlo fino a due settimane dopo la ripresa completa della mobilità. Per evitare gravidanze indesiderate si deve utilizzare un altro metodo contraccettivo.
Se Briladona non è stato interrotto prima, deve essere preso in considerazione un trattamento antitrombotico.
|
|
Anamnesi familiare positiva (tromboembolia venosa in un fratello o un genitore, specialmente in età relativamente giovane, cioè prima dei 50 anni).
|
Se si sospetta una predisposizione ereditaria, la donna deve essere inviata a uno specialista per un parere prima di decidere l'assunzione di qualsiasi COC
|
|
Altre condizioni mediche associate a TEV
|
Cancro, lupus eritematoso sistemico, sindrome emolitica uremica, malattie intestinali infiammatorie croniche (malattia di Crohn o colite ulcerosa) e anemia falciforme
|
|
Età avanzata
|
In particolare al di sopra dei 35 anni
|
Non vi è accordo sul possibile ruolo delle vene varicose e della tromboflebite superficiale nell'esordio e nella progressione della trombosi venosa.
Il maggior rischio di tromboembolia in gravidanza, in particolare nel periodo di 6 settimane del puerperio, deve essere preso in considerazione (per informazioni su “Gravidanza e allattamento” vedere paragrafo 4.6).
Sintomi di TEV (trombosi venosa profonda ed embolia polmonare)
Nel caso si presentassero sintomi di questo tipo, le donne devono rivolgersi immediatamente a un medico e informarlo che stanno assumendo un COC.
I sintomi di trombosi venosa profonda (TVP) possono includere:
- gonfiore unilaterale della gamba e/o del piede o lungo una vena della gamba;
- dolore o sensibilità alla gamba che può essere avvertito solo in piedi o camminando,
- maggiore sensazione di calore nella gamba colpita; pelle della gamba arrossata o con colorazione anomala.
I sintomi di embolia polmonare (EP) possono includere:
- comparsa improvvisa e inspiegata di dispnea e di respirazione accelerata;
- tosse improvvisa che può essere associata a emottisi;
- dolore acuto al torace;
- stordimento grave o capogiri;
- battito cardiaco accelerato o irregolare.
Alcuni di questi sintomi (ad es. “dispnea” e “tosse”) sono aspecifici e possono essere interpretati erroneamente come eventi più comuni o meno gravi (ad es. infezioni delle vie respiratorie).
Altri segni di occlusione vascolare possono includere: dolore improvviso, gonfiore o colorazione blu pallida di un'estremità.
Se l'occlusione ha luogo nell'occhio i sintomi possono variare da offuscamento indolore della vista fino a perdita della vista. Talvolta la perdita della vista avviene quasi immediatamente.
Rischio di tromboembolia arteriosa (TEA)
Studi epidemiologici hanno associato l'uso dei COC a un aumento del rischio di tromboembolie arteriose (infarto miocardico) o di incidenti cerebrovascolari (ad es. attacco ischemico transitorio, ictus). Gli eventi tromboembolici arteriosi possono essere fatali.
Fattori di rischio di TEA
Il rischio di complicanze tromboemboliche arteriose o di un incidente cerebrovascolare nelle donne che utilizzano COC aumenta in presenza di fattori di rischio (vedere la tabella). Briladona è controindicato se una donna presenta un fattore di rischio grave o più fattori di rischio di TEA che la pongono a un maggiore rischio di trombosi arteriosa (vedere paragrafo 4.3). Se una donna presenta più di un fattore di rischio, è possibile che l'aumento del rischio sia maggiore della somma dei singoli fattori; in questo caso deve essere considerato il suo rischio totale. Se si ritiene che il rapporto beneficio/rischio sia negativo, non si deve prescrivere un COC (vedere paragrafo 4.3).
Fattori di rischio di TEA
|
Fattore di rischio
|
Commento
|
|
Età avanzata
|
In particolare al di sopra dei 35 anni
|
|
Fumo
|
Alle donne deve essere consigliato di non fumare se desiderano usare un COC. Alle donne di età superiore a 35 anni che continuano a fumare deve essere vivamente consigliato l'uso di un metodo contraccettivo diverso.
|
|
Ipertensione
|
|
|
Obesità (indice di massa corporea superiore a 30 kg/m2)
|
Il rischio aumenta considerevolmente all'aumentare dell'IMC.
Particolarmente importante nelle donne con altri fattori di rischio
|
|
Anamnesi familiare positiva (tromboembolia arteriosa in un fratello o un genitore, specialmente in età relativamente giovane, cioè prima dei 50 anni).
|
Se si sospetta una predisposizione ereditaria, la donna deve essere inviata a uno specialista per un parere prima di decidere l'assunzione di qualsiasi COC
|
|
Emicrania
|
Un aumento della frequenza o della gravità dell'emicrania durante l'uso di COC (che può essere prodromico di un evento cerebrovascolare) può rappresentare un motivo di interruzione immediata
|
|
Altre condizioni mediche associate ad eventi vascolari avversi
|
Diabete mellito, iperomocisteinemia, valvulopatia e fibrillazione atriale, dislipoproteinemia e lupus eritematoso sistemico.
|
Sintomi di TEA
Nel caso si presentassero sintomi di questo tipo, le donne devono rivolgersi immediatamente a un medico e informarlo che stanno assumendo un COC.
I sintomi di incidente cerebrovascolare possono includere:
- intorpidimento o debolezza improvvisa del viso, di un braccio o di una gamba, soprattutto su un lato del corpo;
- improvvisa difficoltà a camminare, capogiri, perdita dell'equilibrio o della coordinazione;
- improvvisa confusione, difficoltà di elocuzione o di comprensione;
- improvvisa difficoltà a vedere con uno o con entrambi gli occhi;
- improvvisa emicrania, grave o prolungata, senza causa nota;
- perdita di conoscenza o svenimento con o senza convulsioni.
Sintomi temporanei suggeriscono che si tratti di un attacco ischemico transitorio (TIA).
I sintomi di infarto miocardico (IM) possono includere:
- dolore, fastidio, pressione, pesantezza, sensazione di schiacciamento o di pienezza al torace, a un braccio o sotto lo sterno;
- fastidio che si irradia a schiena, mascella, gola, braccia, stomaco;
- sensazione di pienezza, indigestione o soffocamento;
- sudorazione, nausea, vomito o capogiri;
- estrema debolezza, ansia o mancanza di respiro;
- battiti cardiaci accelerati o irregolari.
Adenoma epatico
In rari casi, nelle utilizzatrici di contraccettivi orali combinati sono stati segnalati tumori benigni del fegato e in casi ancora più rari tumori maligni del fegato. In casi isolati, questi tumori hanno determinato emorragie intra-addominali potenzialmente mortali. Nelle donne che assumono contraccettivi orali combinati deve essere preso in considerazione un tumore epatico nella diagnosi differenziale di forte dolore alla parte superiore dell'addome, ingrossamento del fegato o segni di emorragia intra-addominale.
Cancro al seno
Una meta-analisi di 54 studi epidemiologici ha mostrato un leggero aumento del rischio relativo (RR = 1,24) di cancro al seno nelle donne che attualmente stanno usando contraccettivi orali combinati. Il rischio aumentato può essere dovuto ad una diagnosi precoce di carcinoma mammario nelle utilizzatrici di contraccettivi orali combinati, agli effetti biologici dei contraccettivi orali combinati o a una combinazione di entrambi. I carcinomi mammari diagnosticati nelle utilizzatrici di contraccettivi orali combinati o in donne che hanno usato contraccettivi orali combinati negli ultimi 10 anni, sono più localizzati rispetto a quelli diagnosticati nelle donne che non hanno mai utilizzato tali medicinali.
Il cancro al seno è raro tra le donne sotto 40 anni di età che assumano o meno contraccettivi orali combinati. Mentre questo rischio di fondo aumenta con l'età, l'incremento di diagnosi di cancro al seno in utilizzatrici attuali e recenti di contraccettivi orali combinati è piccolo in relazione al rischio globale di cancro al seno (vedere grafico di seguito).
Il fattore di rischio più importante per il cancro al seno nelle utilizzatrici di contraccettivi orali combinati è l'età a cui le donne interrompono l'assunzione di contraccettivi orali combinati; maggiore è l'età, maggiori sono le diagnosi di cancro al seno. La durata dell'uso è meno importante e l'aumento del rischio scompare gradualmente nel corso di 10 anni dopo l'interruzione dell'uso di contraccettivi orali combinati, al punto che a 10 anni sembra non esserci aumento.
Il possibile aumento del rischio di cancro al seno dovrebbe essere discusso con l'utente e ponderato contro i benefici di contraccettivi orali combinati tenendo conto dell'evidenza che essi offrono una protezione sostanziale contro il rischio di sviluppare alcuni altri tumori (ad esempio, ovarico e cancro dell'endometrio).
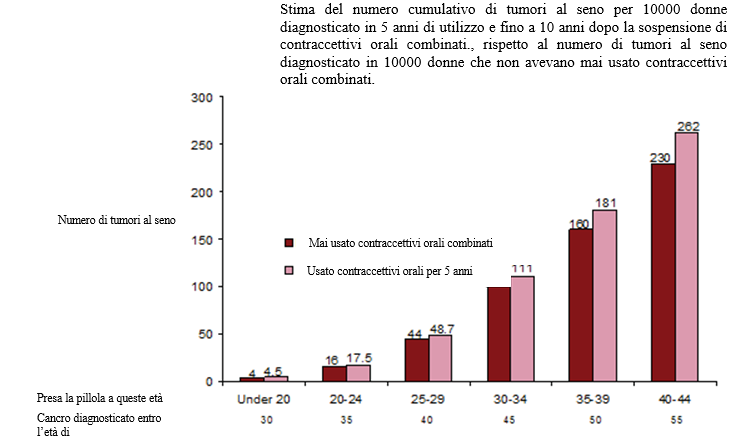
Cancro della cervice
In alcuni studi epidemiologici è stato segnalato, nelle utilizzatrici a lungo termine di contraccettivi orali combinati (> 5 anni), un aumentato rischio di cancro della cervice, tuttavia continua a non esservi consenso su quanto questo risultato sia attribuibile all'influenza di fattori confondenti come il comportamento sessuale e il papilloma virus umano (HPV).
Altri tumori
Con l'uso di contraccettivi orali combinati a più alto dosaggio (50 µg etinilestradiolo) il rischio di cancro dell'endometrio e alle ovaie è ridotto. Se questo valga anche per contraccettivi orali combinati a basso dosaggio resta da confermare.
Sanguinamento irregolare
Con l'assunzione di tutti i contraccettivi orali può verificarsi sanguinamento da sospensione, macchie di sangue e/o assenza di flusso , specialmente durante i primi tre mesi di utilizzo.
Se le irregolarità di sanguinamento persistono oltre i tre cicli o avvengono dopo cicli precedentemente regolari, devono essere prese in considerazione cause non ormonali e adeguate misure diagnostiche sono indicate per escludere un'eventuale neoplasia o gravidanza.
In alcune donne l'emorragia da sospensione può non avvenire durante la fase dell'intervallo senza compresse. Se il contraccettivo orale combinato è stato assunto secondo le indicazioni descritte al paragrafo 4.2, è improbabile che la donna sia incinta. Se, invece, il contraccettivo orale combinato non è stato assunto secondo queste indicazioni prima della prima emorragia da sospensione mancata o se sono mancate due emorragie da sospensione, deve essere esclusa la gravidanza prima di continuare a usare il contraccettivo orale combinato.
Altre condizioni
- Le donne con ipertrigliceridemia o un'anamnesi familiare di tale malattia possono avere un rischio maggiore di pancreatite durante l'uso di contraccettivi orali combinati.
- Anche se sono stati riportati piccoli aumenti della pressione arteriosa in molte donne che assumono contraccettivi orali combinati, aumenti clinicamente rilevanti sono rari. Solo in questi rari casi è giustificata un'interruzione immediata dell'uso dei contraccettivi orali combinati. Se, durante l'uso di un contraccettivo orale combinato con pre-esistente ipertensione, valori di pressione arteriosa costantemente elevati o un aumento significativo della pressione arteriosa non rispondono adeguatamente al trattamento ipertensivo, il contraccettivo orale combinato deve essere sospeso. Se appropriato, l'uso del contraccettivo orale combinato può essere ripreso qualora si riescano a ottenere valori normali con una terapia antipertensiva.
- È stata segnalata l'insorgenza o il peggioramento delle seguenti malattie durante la gravidanza e durante l'uso di contraccettivi orali combinati, ma l'evidenza di un'associazione con l'uso di contraccettivi orali combinati non è conclusiva: ittero e/o prurito correlato a colestasi, calcoli biliari, porfiria, lupus eritematoso sistemico, sindrome uremica emolitica, Corea di Sydenham, herpes gestazionale e perdita dell'udito correlata ad otosclerosi.
- Gli estrogeni esogeni possono indurre o esacerbare i sintomi di angioedema ereditario e acquisito.
- I disturbi acuti o cronici della funzione epatica possono necessitare la sospensione dell'uso di contraccettivi orali combinati fino alla normalizzazione dei marcatori della funzione epatica. La ricorrenza di ittero colestatico e/o prurito correlato a colestasi che si è verificato precedentemente durante la gravidanza o durante l'uso pregresso di steroidi sessuali necessita la sospensione dei contraccettivi orali combinati.
- Sebbene i contraccettivi orali combinati possano avere un effetto sulla resistenza periferica all'insulina e la tolleranza al glucosio, non c'è evidenza di una necessità di modificare il regime terapeutico nelle pazienti diabetiche usando contraccettivi orali combinati a basso dosaggio (contenenti < 0,05 mg di etinilestradiolo). Tuttavia, le donne diabetiche devono essere monitorate attentamente, in particolare nei primi periodi di utilizzo di contraccettivi orali combinati.
- È stato segnalato il peggioramento dell'epilessia, del morbo di Crohn e della colite ulcerosa durante l'uso di contraccettivi orali combinati.
- Occasionalmente può verificarsi cloasma, specialmente nelle donne con un'anamnesi di cloasma gravidico. Le donne con una tendenza al cloasma devono evitare l'esposizione al sole e ai raggi ultravioletti mentre assumono contraccettivi orali combinati.
- L'umore depresso e la depressione sono effetti indesiderati ben noti dell'uso di contraccettivi ormonali (vedere paragrafo 4.8). La depressione può essere grave ed è un fattore di rischio ben noto per il comportamento suicidario e il suicidio. Alle donne va consigliato di contattare il medico in caso di cambiamenti d'umore e sintomi depressivi, anche se insorti poco dopo l'inizio del trattamento.
Eccipienti
Questo medicinale contiene lattosio. Le pazienti affette da rari problemi ereditari di intolleranza al galattosio, da deficit totale di lattasi o da malassorbimento di glucosio-galattosio non devono prendere questo medicinale.
Interazioni con altri medicinali e altre forme di interazione
Quali farmaci o alimenti possono modificare l'effetto di Briladona
Riduzione potenziale dell'efficacia contraccettiva associata alla co-somministrazione di altri farmaci:
Nota: per identificare potenziali interazioni, devono essere consultate le informazioni relative ad altri medicinali assunti contemporaneamente.
Effetti di altri medicinali su Briladona
Le interazioni possono verificarsi con medicinali che inducono gli enzimi microsomiali che possono determinare un aumento nella clearance degli ormoni sessuali e che possono portare a sanguinamento da sospensione e/o al fallimento della contraccezione.
Gestione
L'induzione enzimatica può già essere osservata dopo pochi giorni di trattamento. L'induzione enzimatica massima si vede generalmente entro poche settimane. Dopo la cessazione della terapia farmacologica, l'induzione enzimatica può essere mantenuta per circa 4 settimane.
Trattamento a breve termine
Le donne in trattamento con medicinali a induzione enzimatica devono utilizzare temporaneamente un metodo barriera o un altro metodo di contraccezione in aggiunta ai contraccettivi orali combinati. Il metodo barriera deve essere usato per tutto il tempo della terapia concomitante e per 28 giorni dopo la sua interruzione. Se la terapia prosegue dopo la fine delle compresse nel blister di contraccettivi orali combinati, deve essere iniziato subito il blister di contraccettivi orali combinati successivo senza il consueto intervallo libero da compresse.
Trattamento a lungo termine
Per le donne in trattamento a lungo termine con principi attivi ad induzione enzimatica si raccomanda l'uso di un altro metodo contraccettivo affidabile e non-ormonale.
In letteratura sono state riportate le seguenti interazioni.
Sostanze che aumentano la clearance dei contraccettivi orali combinati (diminuita efficacia dei contraccettivi orali combinati mediante induzione enzimatica), per esempio:
Barbiturici, bosentan, carbamazepina, fenitoina, primidone, rifampicina, e farmaci per il trattamento dell'HIV come ritonavir, nevirapina ed efavirenz e probabilmente anche felbamato, griseofulvina, oxcarbazepina, topiramato e prodotti contenenti il rimedio erboristico Erba di San Giovanni (Hypericum perforatum).
Sostanze con effetti variabili sulla clearance dei contraccettivi orali combinati:
Quando vengono somministrate contemporaneamente a contraccettivi orali combinati, molte combinazioni di inibitori della proteasi dell'HIV e inibitori non-nucleosidici della trascrittasi inversa, tra cui combinazioni con inibitori di HCV, possono aumentare o diminuire le concentrazioni plasmatiche di estrogeni o progestinici. L'effetto netto di questi cambiamenti può essere clinicamente rilevante in alcuni casi.
Pertanto, devono essere consultate le informazioni sulla prescrizione di medicinali concomitanti contro HIV/HCV per identificare potenziali interazioni e le eventuali relative raccomandazioni. In caso di dubbio, le donne in terapia con inibitori della proteasi o inibitori non-nucleosidici della trascrittasi inversa devono utilizzare un metodo contraccettivo di barriera supplementare.
Sostanze che diminuiscono la clearance dei contraccettivi orali combinati (inibitori enzimatici):
La rilevanza clinica di una potenziale interazione con gli inibitori enzimatici rimane sconosciuta.
La somministrazione concomitante di potenti inibitori del CYP3A4 può aumentare le concentrazioni plasmatiche degli estrogeni o dei progestinici o di entrambi.
Dosi di etoricoxib da 60 a 120 mg/die hanno dimostrato di aumentare le concentrazioni plasmatiche di etinilestradiolo rispettivamente da 1,4 a 1,6 volte, quando somministrate in concomitanza con un contraccettivo ormonale combinato contenente 0,035 mg di etinilestradiolo.
Effetti di Briladona su altri medicinali
I contraccettivi orali combinati possono interferire sul metabolismo di altri principi attivi.
Di conseguenza, le concentrazioni plasmatiche e tissutali possono aumentare (ad es. ciclosporina) o diminuire (ad es. lamotrigina).
Dati clinici suggeriscono che l'etinilestradiolo inibisce la clearance dei substrati del CYP1A2 portando ad un debole (per es. teofillina) o moderato (per. es. tizanidina) aumento delle loro concentrazioni plasmatiche.
Interazioni farmacodinamiche
Durante gli studi clinici con pazienti trattati per le infezioni da virus dell'epatite C (HCV) con medicinali contenenti ombitasvir/paritaprevir/ritonavir e dasabuvir con o senza ribavirina, si sono verificati in maniera significativa aumenti delle transaminasi (ALT) superiori a 5 volte il limite superiore della norma (ULN) più frequentemente nelle donne che utilizzavano medicinali contenenti etinilestradiolo come i contraccettivi ormonali combinati (COC). Inoltre, anche nei pazienti trattati con glecaprevir/pibrentasvir o sofosbuvir/velpatasvir/voxilaprevir, sono stati osservati aumenti delle ALT in donne che usavano farmaci contenenti etinilestradiolo
come i COC (vedere paragrafo 4.3).
Pertanto, le utilizzatrici di Briladona devono passare a un metodo contraccettivo alternativo (per esempio contraccezione a base di solo progestinico o metodi non ormonali) prima di iniziare la terapia con questi regimi farmacologici combinati. Briladona può essere ricominciato 2 settimane dopo la fine del trattamento con questi regimi combinati di medicinali.
Test di laboratorio
L'uso di steroidi contraccettivi può influenzare i risultati di alcuni esami di laboratorio, compresi parametri biochimici di fegato, tiroide, corteccia surrenale e della funzione renale, livelli plasmatici delle proteine (di trasporto), per es. globuline legate a corticosteroidi e frazioni lipido/lipoproteiche, parametri del metabolismo dei carboidrati e parametri della coagulazione e della fibrinolisi. Le variazioni rimangono generalmente entro i normali limiti di laboratorio.
Interazioni riportate su letteratura scientifica internazionale
Prima di prendere "Briladona" insieme ad altri farmaci come “Aprepitant Accord”, “Aprepitant Teva”, “Atanto”, “Atazanavir Krka”, “Atazanavir Mylan”, “Atazanavir Sandoz”, “Aurantin - Soluzione (uso Interno)”, “Braftovi”, “Carbamazepina EG”, “Carbamazepina Zentiva - Compressa A Rilascio Modificato”, “Dintoinale”, “Dotecine”, “Edeven C.M.”, “Efavirenz E Emtricitabina E Tenofovir Disoproxil Aurobindo”, “Efavirenz + Emtricitabina + Tenofovir Disoproxil Mylan”, “Efavirenz Emtricitabina Tenofovir Disoproxil Krka”, “Efavirenz Emtricitabina Tenofovir Disoproxil Teva”, “Efavirenz / Emtricitabina / Tenofovir Disoproxil Zentiva”, “Emend”, “Essaven Gel”, “Evotaz”, “Fenitoina Hikma”, “Fenobarbitale Sodico Salf”, “Fosaprepitant Hikma”, “Fulcin”, “Gamibetal Complex”, “Gardenale”, “Ivemend”, “Liotontrauma”, “Luminale - Compressa”, “Maviret - Compresse Rivestite”, “Maviret - Granulato”, “Mycobutin”, “Mysoline”, “Nervaxon”, “Nevirapina Mylan”, “Nevirapina Teva Italia”, “Oxcarbazepina Tecnigen - Compresse Rivestite”, “Reparil”, “Reparilexin”, “Reyataz - Capsula”, “Rifadin”, “Rifater”, “Rifinah”, “Rifocin”, “Somatoline - Emulsione”, “Somatoline - Gel”, “Stadmycin”, “Targretin”, “Tegretol”, “Tolep”, “Viramune”, “Vosevi”, “Zigabal - Compressa”, etc.., chiedi al tuo al tuo medico o farmacista di fiducia di verificare che sia sicuro e non dannoso per la tua salute ...
Fertilità, gravidanza e allattamento
Gravidanza
Se durante l'assunzione di Briladona si verifica una gravidanza, il medicinale deve essere immediatamente sospeso. Approfonditi studi epidemiologici non hanno rilevato né un aumento del rischio di difetti alla nascita nei bambini nati da donne che hanno usato contraccettivi orali combinati contenenti etinilestradiolo prima della gravidanza, né un effetto teratogeno quando contraccettivi orali combinati contenenti etinilestradiolo sono stati presi inavvertitamente durante le prime fasi della gravidanza.
Il maggior rischio di TEV nel periodo dopo il parto deve essere preso in considerazione quando viene ripresa l'assunzione di Briladona (vedere paragrafi 4.2 e 4.4).
Allattamento
L'allattamento può essere influenzato dai contraccettivi orali combinati in quanto possono ridurre la quantità e modificare la composizione del latte materno. Perciò, l'uso di contraccettivi orali combinati generalmente non deve essere raccomandato finché la madre che allatta al seno non abbia completamente svezzato il figlio. Piccole quantità di steroidi contraccettivi e/o di loro metaboliti possono essere escrete nel latte materno durante l'uso di contraccettivi orali combinati. Queste quantità possono influire sul bambino.
Fertilità
Briladona è indicato per la prevenzione della gravidanza. Per informazioni sul ritorno alla fertilità, vedere paragrafo 5.1
Effetti sulla capacità di guidare veicoli e sull'uso di macchinari
Non sono stati effettuati studi sugli effetti sulla capacità di guidare veicoli e sull'uso di macchinari. Non sono stati osservati effetti sulla capacità di guidare e sull'uso di macchinari nelle utilizzatrici di COC.
Effetti indesiderati
Quali sono gli effetti collaterali di Briladona
Riassunto del profilo di sicurezza
Un rischio aumentato di eventi trombotici e tromboembolici arteriosi e venosi, compreso infarto miocardico, ictus, attacchi ischemici transitori, trombosi venosa ed embolia polmonare sono stati osservati in donne che usano COC. Questi sono discussi più dettagliatamente nel paragrafo 4.4.
Nella tabella seguente vengono visualizzati tutte le reazioni avverse che sono state segnalate con l'utilizzo di Briladona nelle sperimentazioni cliniche o da esperienze post-marketing con compresse di norgestimato ed etinilestradiolo.
Le categorie di frequenze visualizzate utilizzano la seguente convenzione: molto comune (> 1/10); comune (> 1/100 a < 1/10); non comune (> 1/1000 a < 1/100); rare (> 1/10000 a < 1/1000); molto raro (< 1/10000); e frequenza non nota (non può essere definita sulla base dei dati disponibili):
|
Classificazione per sistemi e organi
|
Molto comune
(> 1/10)
|
Comune
(da ≥1/100 a <10)
|
Non comune da
(≥ 1/1.000 a <1/100)
|
Raro
(da ≥ 1/10.000 a < 1/1.000)
|
Molto raro
(<1/10000)
|
Non noto
|
|
Infezioni e infestazioni
|
|
Infezioni del tratto urinario,
infezioni vaginali
|
|
|
|
|
|
Neoplasie benigne, maligne e non specificate (comprese le cisti e polipi)
|
|
|
Displasia della cervice
|
Cisti al seno
|
|
Adenoma epatico,
cancro al seno,
neoplasia benigna al seno,
iperplasia focale nodulare,
fibroadenoma al seno
|
|
Disturbi del sistema immunitario
|
|
Ipersensibilità
|
|
|
|
Esacerbazione dei sintomi di angioedema ereditario e acquisito
|
|
Disturbi della nutrizione e del metabolismo
|
|
Ritenzione di fluidi
|
Aumento e diminuzione dell'appetito,
variazioni del peso
|
|
|
Dislipidemia
|
|
Disturbi psichiatrici
|
|
Alterazioni dell'umore,
depressione,
nervosismo,
insonnia
|
Ansia,
disturbi del desiderio sessuale
|
|
|
|
|
Patologie del sistema nervoso
|
Cefalea
|
Emicrania,
Capogiri
|
Sincope,
parestesia
|
|
|
Incidente cerebrovascolare, convulsione
|
|
Patologie dell'occhio
|
|
|
Compromissione della visione, occhio secco
|
|
|
Intolleranza alle lenti a contatto, trombosi vascolare retinica *
|
|
Disturbi dell'orecchio e del labirinto
|
|
|
|
Vertigini
|
|
|
|
Disturbi cardiaci
|
|
|
Palpitazioni
|
Tachicardia
|
|
Infarto miocardico
|
|
Disordini vascolari
|
|
|
Trombosi,
ipertensione,
vampate di calore
|
Tromboembolismo venoso,
Tromboembolismo arterioso
|
|
Trombosi venosa profonda *, trombosi venosa * *
|
|
Disturbi respiratori, toracici e mediastinici
|
|
|
Dispnea
|
|
|
Embolia polmonare *
|
|
Patologie gastrointestinali
|
Disturbi gastrointestinali,
vomito,
diarrea,
nausea
|
Dolore gastrointestinale,
dolore addominale,
distensione addominale,
costipazione,
flatulenza
|
|
Pancreatite
|
|
|
|
Disturbi epato-biliari
|
|
|
|
Epatiti
|
|
|
|
Patologia della cute e del tessuto sottocutaneo
|
|
Acne,
Eruzione cutanea
|
Alopecia,
irsutismo,
Orticaria,
prurito,
eritema,
decolorazione della pelle
|
Iperidrosi,
reazione di fotosensibilità
|
|
Angioedema,
eritema nodoso,
sudorazioni notturne
|
|
Patologie muscolo-scheletriche e del tessuto connettivo
|
|
Spasmi muscolari,
dolore alle estremità,
mal di schiena
|
Mialgia
|
|
|
|
|
Patologie dell'apparato riproduttivo e della mammella
|
Dismenorrea, metrorragia, emorragia da sospensione anormale
|
Amenorrea,
secrezione genitale,
dolore mammario
|
Secrezioni mammarie
Aumento del volume mammario,
ciste ovarica,
secchezza vulvovaginale
|
Secrezione vaginale
|
|
Soppressione della lattazione
|
|
Disturbi generici ed al sito di somministrazione
|
|
Dolore al petto,
edema,
condizioni asteniche
|
|
|
|
|
|
Esami diagnostici
|
|
Aumento del peso
|
Diminuzione del peso
|
|
|
|
* Non visto in studi clinici pertanto la frequenza non può essere definita. Vedere il paragrafo 4.4 per la frequenza in base ai tassi di segnalazione standard per contraccettivi ormonali combinati simili.
** I termini aggregati per la trombosi venosa comprendono la sindrome di Budd Chiari e la trombosi della vena epatica.
Descrizione di reazioni avverse selezionate
Un aumento del rischio di eventi trombotici e tromboembolici arteriosi e venosi, inclusi infarto miocardico, ictus, attacchi ischemici transitori, trombosi venosa ed embolia polmonare è stato osservato nelle donne che usano COC, e sono discussi in maggior dettaglio nel paragrafo 4.4.
Le seguenti reazioni avverse gravi sono state riportate in donne che utilizzano COC e vengono discusse nel paragrafo 4.4 Avvertenze speciali e precauzioni di impiego:
- Disturbi tromboembolici venosi;
- Disturbi tromboembolici arteriosi;
- Ipertensione;
- Tumori epatici;
- Presenza o peggioramento di condizioni per le quali l'associazione con i COC non è conclusiva: Morbo di Crohn, colite ulcerosa, epilessia, mioma uterino, porfiria, lupus eritematoso sistemico, herpes gestazionale, corea di Sydenham, sindrome emolitico-uremica, ittero colestatico.
- Cloasma;
- Disturbi acuti o cronici della funzionalità epatica possono richiedere l'interruzione dell'uso del COC fino a quando i marker della funzionalità epatica non tornano alla normalità.
La frequenza di diagnosi di tumore al seno è leggermente aumentata nelle donne che utilizzano COC. Poiché il tumore al seno si verifica raramente in donne al di sotto dei 40 anni, il numero di casi aggiuntivi rispetto al rischio complessivo è piccolo. Non è nota la relazione causale con l'uso di COC. Per ulteriori informazioni, vedere paragrafi 4.3. e 4.4.
Interazioni
Un'emorragia da sospensione e/o un fallimento della contraccezione possono essere il risultato di interazioni di altri medicinali (induttori enzimatici) con i contraccettivi orali (vedere paragrafo 4.5).
Segnalazione delle reazioni avverse sospette
La segnalazione delle reazioni avverse sospette che si verificano dopo l'autorizzazione del medicinale è importante, in quanto permette un monitoraggio continuo del rapporto beneficio/rischio del medicinale. Agli operatori sanitari è richiesto di segnalare qualsiasi reazione avversa sospetta tramite il sistema nazionale di segnalazione all'indirizzo www.aifa.gov.it/content/segnalazioni-reazioni-avverse.
Sovradosaggio
Cosa fare se avete preso una dose eccessiva di Briladona
Non ci sono segnalazioni di effetti indesiderati gravi da sovradosaggio. I sintomi che possono verificarsi sono: nausea, vomito e sanguinamento vaginale. Non ci sono antidoti specifici. Il trattamento dovrà essere sintomatico.
Scadenza
2 anni
Conservazione
Conservare a temperatura inferiore ai 30ºC
Conservare il blister nell'imballaggio esterno per proteggere il medicinale dalla luce.
Elenco degli eccipienti
Amido di mais
Lattosio monoidrato
Magnesio stearato
carminio d'indaco (E132)


