Azelastina E Fluticasone EG
Ultimo aggiornamento: 28/03/2024
Cos'è Azelastina E Fluticasone EG?
Azelastina E Fluticasone EG è un farmaco a base del principio attivo
Azelastina + Fluticasone, appartenente alla categoria degli
Antiallergici e nello specifico
Corticosteroidi. E' commercializzato in Italia dall'azienda
EG S.p.A. - Società del Gruppo STADA Arzmeimittel AG.
Azelastina E Fluticasone EG può essere prescritto con Ricetta RR - medicinali soggetti a prescrizione medica.
Azelastina E Fluticasone EG può essere prescritto con Ricetta RR - medicinali soggetti a prescrizione medica.
Confezioni
Azelastina e fluticasone EG 137 microgrammi/50 microgrammi spray nasale sosp. 1 flacone 23 g/120 erogazioni
Informazioni commerciali sulla prescrizione
Titolare: EG S.p.A. - Società del Gruppo STADA Arzmeimittel AG
Ricetta: RR - medicinali soggetti a prescrizione medica
Classe: C
Principio attivo: Azelastina + Fluticasone
Gruppo terapeutico: Antiallergici
ATC: R01AD58 - Fluticasone, associazioni
Forma farmaceutica: spray
Ricetta: RR - medicinali soggetti a prescrizione medica
Classe: C
Principio attivo: Azelastina + Fluticasone
Gruppo terapeutico: Antiallergici
ATC: R01AD58 - Fluticasone, associazioni
Forma farmaceutica: spray
Se sei un professionista, potrai trovare le schede tecniche complete e molto altro nell'area riservata di Codifa.it
Indicazioni
Perché si usa Azelastina E Fluticasone EG? A cosa serve?
Sollievo dai sintomi della rinite allergica stagionale e perenne da moderata a grave, quando la monoterapia con antistaminico o glucocorticoide per via intra-nasale non è ritenuta sufficiente.
Posologia
Come usare Azelastina E Fluticasone EG: Posologia
Posologia
Per ottenere un beneficio terapeutico completo, è essenziale un uso regolare. Evitare il contatto con gli occhi.
Adulti e adolescenti (da 12 anni di età)
Un'erogazione in ogni narice due volte al giorno (mattino e sera).
Bambini con meno di 12 anni di età
L'uso di Azelastina + Fluticasone EG spray nasale non è raccomandato in bambini di età inferiore a 12 anni, poiché la sicurezza e l'efficacia in questa popolazione di pazienti non sono ancora state stabilite.
Anziani
In questa popolazione di pazienti, non è richiesto alcun aggiustamento della dose.
Compromissione renale ed epatica
Non sono disponibili dati sui pazienti con compromissione renale ed epatica.
Durata del trattamento
Azelastina e Fluticasone EG spray nasale è indicato per un uso a lungo termine.
La durata del trattamento deve corrispondere al periodo di esposizione agli allergeni.
Modo di somministrazione
Azelastina e Fluticasone EG spray nasale è indicato solo per uso nasale.
Istruzioni per l'uso
Preparazione dello spray:
Il flacone deve essere agitato delicatamente prima dell'uso per circa 5 secondi, inclinandolo verso il basso e verso l'alto e successivamente occorre togliere il cappuccio protettivo. Prima di usare Azelastina e Fluticasone EG spray nasale per la prima volta, occorre premere la pompa verso il basso e rilasciarla per 6 volte. Se Azelastina e Fluticasone EG spray nasale non è stato usato da più di 7 giorni, è necessario ricaricare la pompa una volta, premendola verso il basso e rilasciandola.
Uso dello spray:
Il flacone deve essere agitato delicatamente prima dell'uso per circa 5 secondi, inclinandolo verso il basso e verso l'alto e successivamente occorre togliere il cappuccio protettivo.
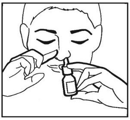
Dopo aver soffiato il naso, spruzzare la sospensione una volta in ciascuna narice, tenendo la testa inclinata verso il basso (vedere la figura). Dopo l'uso è necessario asciugare l'ugello dello spray e riposizionare il cappuccio protettivo.
Controindicazioni
Quando non dev'essere usato Azelastina E Fluticasone EG
Ipersensibilità ai principi attivi o a uno qualsiasi degli eccipienti elencati al paragrafo 6.1.
Avvertenze speciali e precauzioni di impiego
Cosa serve sapere prima di prendere Azelastina E Fluticasone EG
Durante l'utilizzo post-marketing, sono state segnalate interazioni farmacologiche clinicamente significative in pazienti a cui sono stati somministrati fluticasone propionato e ritonavir, con conseguenti effetti sistemici dei corticosteroidi, incluse sindrome di Cushing e soppressione surrenalica. Deve essere pertanto evitata la co-somministrazione di fluticasone propionato e ritonavir, a meno che il beneficio potenziale per il paziente non superi il rischio di effetti indesiderati sistemici dei corticosteroidi (vedere paragrafo 4.5).
Gli effetti sistemici dei corticosteroidi somministrati per via nasale possono manifestarsi soprattutto quando sono prescritti a dosi elevate per periodi prolungati. Essi possono variare nei singoli pazienti e fra diverse preparazioni di corticosteroidi ma rispetto ai corticosteroidi orali la loro insorgenza è assai meno probabile. I potenziali effetti sistemici possono includere sindrome di Cushing, aspetto Cushingoide, soppressione surrenalica, ritardo della crescita in bambini e adolescenti, cataratta, glaucoma e più raramente, una serie di effetti psicologici o comportamentali, fra cui iperattività psicomotoria, disturbi del sonno, ansia, depressione o aggressività (soprattutto nei bambini).
Lo spray nasale a base di azelastina cloridrato/fluticasone propionato è sottoposto a esteso metabolismo di primo passaggio, pertanto in pazienti con epatopatia severa è probabile un'aumentata esposizione sistemica di fluticasone propionato intra-nasale. Questa condizione può comportare una maggiore frequenza di eventi avversi sistemici.
Si raccomanda cautela in questi pazienti.
Un trattamento con dosi di corticosteroidi per via nasale superiori a quelle raccomandate può provocare una soppressione surrenalica clinicamente significativa. Se vi è evidenza di utilizzo di dosi superiori a quelle raccomandate, occorre prendere in considerazione una copertura aggiuntiva con corticosteroidi sistemici durante periodi di stress o in caso di chirurgia elettiva.
In generale, la dose di fluticasone intra-nasale deve essere ridotta alla dose più bassa in grado di controllare efficacemente i sintomi della rinite. Dosi superiori a quella raccomandata (vedere paragrafo 4.2) non sono state testate per azelastina cloridrato/fluticasone propionato. Analogamente a tutti i corticosteroidi intra- nasali, è necessario prendere in considerazione il carico sistemico totale dei corticosteroidi, ogni volta che vengono prescritte altre forme concomitanti di trattamento a base di corticosteroidi.
In bambini trattati con corticosteroidi per via nasale alle dosi autorizzate, è stato riportato un ritardo della crescita. Poiché la crescita si verifica anche negli adolescenti, si raccomanda di monitorare regolarmente anche la crescita degli adolescenti che ricevono un trattamento prolungato con corticosteroidi per via nasale. In caso di rallentamento della crescita, è necessario rivalutare la terapia con l'obiettivo, se possibile, di ridurre la dose del corticosteroide per uso nasale al livello più basso in grado di controllare efficacemente i sintomi.
Con l'uso di corticosteroidi sistemici e topici possono essere riferiti disturbi visivi. Se un paziente manifesta sintomi come visione offuscata o altri disturbi visivi, è necessario considerare il rinvio a un oculista per la valutazione delle possibili cause che possono includere cataratta, glaucoma o malattie rare come la corioretinopatia sierosa centrale (CSCR), che sono state segnalate dopo l'uso di corticosteroidi sistemici e topici.
È necessario un attento monitoraggio in pazienti con alterazioni della vista o con storia di aumento della pressione oculare, glaucoma e/o cataratta.
Nel caso in cui sussista qualsiasi motivo per ritenere che la funzionalità surrenalica sia compromessa, occorre prestare attenzione quando i pazienti passano da un trattamento con steroidi sistemici a Azelastina + Fluticasone EG spray nasale.
Nei pazienti affetti da tubercolosi, da qualsiasi tipo di infezione non trattata, o che si sono recentemente sottoposti a intervento chirurgico o con una lesione recente a carico di naso o bocca, i possibili benefici del trattamento con Azelastina e Fluticasone EG spray nasale devono essere valutati rispetto ai possibili rischi.
Le infezioni delle vie aeree nasali devono essere trattate con terapia antibatterica o antimicotica, ma non costituiscono una specifica controindicazione al trattamento con Azelastina e Fluticasone EG spray nasale.
Eccipienti
Questo medicinale contiene 0,014 mg di benzalconio cloruro per erogazione. L'uso prolungato può causare edema della mucosa nasale.
Questo medicinale contiene meno di 1 mmol (23 mg) di sodio per erogazione, cioè essenzialmente ‘senza sodio'.
Interazioni con altri medicinali e altre forme di interazione
Quali farmaci o alimenti possono modificare l'effetto di Azelastina E Fluticasone EG
Fluticasone propionato
In condizioni normali, a seguito di somministrazione per via intranasale, si raggiungono basse concentrazioni plasmatiche di fluticasone propionato; ciò a causa dell'esteso metabolismo di primo passaggio e dell'elevata clearance sistemica nell'intestino e nel fegato, mediati dal citocromo P450 3A4. Pertanto, sono improbabili interazioni clinicamente significative con altri principi attivi mediati dal fluticasone propionato.
Uno studio d'interazione farmacologica, condotto in soggetti sani, ha dimostrato che ritonavir (un potente inibitore del citocromo P450 3A4) può aumentare in modo considerevole le concentrazioni plasmatiche di fluticasone propionato, con conseguente marcata riduzione delle concentrazioni di cortisolo sierico. Durante l'utilizzo post-marketing sono state segnalate interazioni farmacologiche clinicamente significative in pazienti trattati con ritonavir e fluticasone propionato somministrato per via intra-nasale o inalatoria, con conseguenti effetti sistemici da corticosteroidi. Si ritiene che il trattamento concomitante con altri inibitori di CYP3A, compresi i medicinali contenenti cobicistat, possa aumentare il rischio di effetti indesiderati sistemici. L'associazione deve essere evitata a meno che il beneficio non superi il rischio aumentato di effetti indesiderati sistemici dovuti ai corticosteroidi; in questo caso è necessario monitorare i pazienti per gli effetti indesiderati sistemici dovuti ai corticosteroidi.
Studi hanno dimostrato che altri inibitori del citocromo P450 3A4 generano aumenti trascurabili (eritromicina) e di lieve entità (ketoconazolo) nell'esposizione sistemica al fluticasone propionato, senza significative riduzioni delle concentrazioni sieriche di cortisolo. Ciononostante, si raccomanda cautela in caso di co-somministrazione di potenti inibitori del citocromo P450 3A4 (ad esempio, ketoconazolo), poiché sussiste il rischio potenziale di aumento dell'esposizione sistemica al fluticasone propionato.
Azelastina cloridrato
Non sono stati effettuati studi specifici di interazione con azelastina cloridrato spray nasale. Sono stati effettuati studi di interazione a dosi orali elevate. Tuttavia, essi non hanno alcuna rilevanza per azelastina spray nasale, poiché le dosi raccomandate per via nasale determinano un'esposizione sistemica notevolmente inferiore. Occorre tuttavia prestare attenzione, quando si somministra azelastina cloridrato a pazienti che assumono contemporaneamente sedativi o farmaci che agiscono sul sistema nervoso centrale, poiché è possibile che l'effetto sedativo venga potenziato. Anche l'alcool può esacerbare questo effetto (vedere paragrafo 4.7).
Interazioni riportate su letteratura scientifica internazionale
Prima di prendere "Azelastina E Fluticasone EG" insieme ad altri farmaci come “Alcool Idroabietilico Allergeaze”, “Atazanavir Krka”, “Atazanavir Mylan”, “Atazanavir Sandoz”, “Darunavir Accord - Compresse Rivestite”, “Darunavir Aurobindo - Compresse Rivestite”, “Darunavir KRKA - Compresse Rivestite”, “Darunavir Mylan - Compresse Rivestite”, “Darunavir Sandoz - Compresse Rivestite”, “Darunavir Tillomed - Compresse Rivestite”, “Darunavir Zentiva - Compresse Rivestite”, “Evotaz”, “Genvoya”, “Kaletra - Compresse Rivestite”, “Kaletra - Soluzione”, “Lopinavir E Ritonavir Mylan”, “Norvir - Compresse Rivestite”, “Norvir - Polvere Per Sospensione”, “Paxlovid”, “Prezista - Compressa”, “Prezista - Sospensione”, “Reyataz - Capsula”, “Rezolsta”, “Ritonavir Mylan”, “Ritonavir Sandoz”, “Stribild”, “Symtuza”, etc.., chiedi al tuo al tuo medico o farmacista di fiducia di verificare che sia sicuro e non dannoso per la tua salute ...
Fertilità, gravidanza e allattamento
Fertilità
Esiste solo un numero limitato di dati relativi alla fertilità (vedere paragrafo 5.3).
Gravidanza
I dati relativi all'uso di azelastina cloridrato e fluticasone propionato in donne in gravidanza non esistono o sono in numero limitato. Azelastina + Fluticasone EG spray nasale deve essere pertanto utilizzato durante la gravidanza solo se il beneficio potenziale giustifica il rischio potenziale per il feto (vedere paragrafo 5.3).
Allattamento
Non è noto se dopo somministrazione per via nasale, azelastina cloridrato, fluticasone propionato o i loro metaboliti vengano escreti nel latte materno umano. Azelastina e Fluticasone EG spray nasale deve essere usato durante l'allattamento soltanto se il potenziale beneficio giustifica il potenziale rischio per il neonato/bambino.
Effetti sulla capacità di guidare veicoli e sull'uso di macchinari
Azelastina + Fluticasone EG spray nasale altera lievemente la capacità di guidare veicoli e di usare macchinari.
In casi isolati, durante l'uso di Azelastina e Fluticasone EG spray nasale possono manifestarsi affaticamento, stanchezza, spossatezza, capogiro o debolezza, che possono anche essere causati dalla malattia stessa. In questi casi, la capacità di guidare veicoli e usare macchinari può essere compromessa. L'alcool può potenziare questo effetto.
Effetti indesiderati
Quali sono gli effetti collaterali di Azelastina E Fluticasone EG
Di solito, dopo la somministrazione, può manifestarsi disgeusia, un sapore sgradevole tipico del farmaco (spesso a causa di una errata modalità di applicazione, vale a dire reclinando troppo indietro la testa durante la somministrazione).
Gli effetti indesiderati sono elencati di seguito per classe di organo e frequenza. Le frequenze sono definite come:
| Molto comune | (≥1/10) |
| Comune | (≥1/100 - <1/10) |
| Non comune | (≥1/1.000-<1/100) |
| Raro | (≥1/10.000 - <1/1.000) |
| Molto raro | (<1/10.000) |
Non noto (la frequenza non può essere valutata sulla base dei dati disponibili)
|
Frequenza
|
Molto comune
|
Comune
|
Non comune
|
Raro
|
Molto raro
|
Non noto
|
|
Classificazione per sistemi e organi
|
||||||
|
Disturbi del sistema immunitario
|
|
|
|
|
Ipersensibilità, comprese reazioni anafilattiche, angioedema (edema di faccia o lingua e rash cutaneo), broncospasmo
|
|
|
Patologie del sistema nervoso
|
|
Cefalea, disgeusia (sapore sgradevole), odore sgradevole
|
|
|
Capogiro, sonnolenza (sonno, assopimento)
|
|
|
Patologie dell'occhio
|
|
|
|
|
Glaucoma, pressione intraoculare aumentata, cataratta
|
Visione offuscata (vedere anche paragrafo 4.4)
|
|
Patologie respiratorie, toraciche e mediastiniche
|
Epistassi
|
|
Fastidio nasale (inclusi irritazione nasale, dolore pungente, prurito), starnuti, secchezza nasale, tosse, gola secca, irritazione della gola
|
|
Perforazione del setto nasale**, erosione mucosale
|
Ulcere nasali
|
|
Patologie gastrointestinali
|
|
|
|
Bocca secca
|
Nausea
|
|
|
Patologie della cute
e del tessuto sottocutaneo
|
|
|
|
|
Eruzione cutanea, prurito, orticaria
|
|
|
Patologie generali e
condizioni relative alla sede di somministrazione
|
|
|
|
|
Affaticamento
(stanchezza, spossatezza), debolezza (vedere paragrafo 4.7)
|
|
* Dopo il trattamento prolungato con fluticasone propionato per via intranasale, è stato identificato un numero assai ridotto di segnalazioni spontanee.
** È stata riportata la perforazione del setto nasale dopo l'uso di corticosteroidi per via intranasale.
Gli effetti sistemici dei corticosteroidi somministrati per via nasale possono manifestarsi soprattutto quando sono prescritti a dosi elevate per periodi prolungati (vedere paragrafo 4.4).
È stato riportato un ritardo della crescita nei bambini trattati con corticosteroidi per via nasale. Anche negli adolescenti è possibile un ritardo della crescita (vedere paragrafo 4.4).
In rari casi è stata osservata osteoporosi, quando i glucocorticoidi per via nasale sono stati somministrati per periodi prolungati.
Segnalazione delle reazioni avverse sospette
La segnalazione delle reazioni avverse sospette che si verificano dopo l'autorizzazione del medicinale è importante, in quanto permette un monitoraggio continuo del rapporto beneficio/rischio del medicinale. Agli operatori sanitari è richiesto di segnalare qualsiasi reazione avversa sospetta tramite il sistema nazionale di segnalazione all'indirizzo http://www.aifa.gov.it/content/segnalazioni-reazioni-avverse.
Sovradosaggio
Cosa fare se avete preso una dose eccessiva di Azelastina E Fluticasone EG
Non si prevedono reazioni da sovradosaggio con la via di somministrazione nasale.
Non sono disponibili dati da pazienti sugli effetti del sovradosaggio acuto o cronico con fluticasone propionato intra-nasale.
La somministrazione intra-nasale di 2 milligrammi di fluticasone propionato (10 volte la dose giornaliera raccomandata), due volte al giorno per sette giorni in volontari sani, non ha prodotto alcun effetto sulla funzione dell'asse ipotalamo-ipofisi-surrene (HPA).
La somministrazione di dosi più elevate di quelle raccomandate per un lungo arco di tempo può comportare la temporanea soppressione della funzione surrenale.
In questi pazienti, il trattamento con Azelastina + Fluticasone EG spray nasale deve essere continuato alla dose sufficiente per controllare i sintomi. La funzione surrenale riprenderà dopo pochi giorni e può essere verificata misurando il livello di cortisolo plasmatico.
In caso di sovradosaggio dopo accidentale assunzione orale, sulla base dei risultati ottenuti da studi su animali è possibile che si manifestino disturbi del sistema nervoso centrale causati da azelastina cloridrato (tra cui sonnolenza, confusione, coma, tachicardia e ipotensione).
Il trattamento di questi disturbi deve essere sintomatico. Si raccomanda l'esecuzione di una lavanda gastrica, in base al quantitativo ingerito. Non esiste alcun antidoto noto.
Scadenza
2 anni.
Periodo di validità in uso (dopo il primo utilizzo): 6 mesi.
Conservazione
Non refrigerare o congelare.
Foglietto Illustrativo
Fonti Ufficiali
© 2022 EDRA S.p.A. - P.iva 08056040960
DPO - dpo@lswr.it