Tiotropio Teva Italia
Ultimo aggiornamento: 01/06/2023
Cos'è Tiotropio Teva Italia?
Tiotropio Teva Italia è un farmaco a base del principio attivo
Tiotropio Bromuro, appartenente alla categoria degli
farmaci per disturbi ostruttivi delle vie respiratorie, anticolinergici e nello specifico
Anticolinergici. E' commercializzato in Italia dall'azienda
Teva Italia S.r.l. - Sede legale.
Tiotropio Teva Italia può essere prescritto con Ricetta RR - medicinali soggetti a prescrizione medica.
Tiotropio Teva Italia può essere prescritto con Ricetta RR - medicinali soggetti a prescrizione medica.
Confezioni
Tiotropio Teva Italia 10 mcg polvere per inalazione 30 capsule
Informazioni commerciali sulla prescrizione
Titolare: Teva Italia S.r.l. - Sede legale
Ricetta: RR - medicinali soggetti a prescrizione medica
Classe: A
Principio attivo: Tiotropio Bromuro
Gruppo terapeutico: farmaci per disturbi ostruttivi delle vie respiratorie, anticolinergici
ATC: R03BB04 - Tiotropio bromuro
Forma farmaceutica: polvere per inalazione
Ricetta: RR - medicinali soggetti a prescrizione medica
Classe: A
Principio attivo: Tiotropio Bromuro
Gruppo terapeutico: farmaci per disturbi ostruttivi delle vie respiratorie, anticolinergici
ATC: R03BB04 - Tiotropio bromuro
Forma farmaceutica: polvere per inalazione
Se sei un professionista, potrai trovare le schede tecniche complete e molto altro nell'area riservata di Codifa.it
Indicazioni
Perché si usa Tiotropio Teva Italia? A cosa serve?
Tiotropio Teva Italia è indicato come terapia broncodilatatoria di mantenimento per il sollievo dai sintomi in pazienti affetti da broncopneumopatia cronica ostruttiva (BPCO).
Tiotropio Teva Italia è indicato per l'uso negli adulti.
Posologia
Come usare Tiotropio Teva Italia: Posologia
Posologia
Modo di somministrazione: Uso inalatorio.
Dose raccomandata
Adulti di età pari o superiore a 18 anni:
Inalazione del contenuto di una capsula una volta al giorno usando l'inalatore Zonda.
L'inalazione deve essere effettuata ogni giorno alla stessa ora.
La dose raccomandata non deve essere superata.
La dose erogata da una singola capsula (10 microgrammi) è sufficiente ed è la dose normale per la terapia con Tiotropio Teva Italia.
Le capsule di Tiotropio Teva Italia sono esclusivamente per uso inalatorio; non devono essere ingerite.
Le capsule di Tiotropio Teva Italia devono essere inalate esclusivamente utilizzando l'inalatore Zonda.
Popolazioni speciali
I pazienti anziani possono utilizzare Tiotropio Bromuro alla dose raccomandata.
I pazienti con danno renale lieve (clearance della creatinina >50 ml/min) possono utilizzare tiotropio bromuro alla dose raccomandata. Per pazienti con danno renale da moderato a grave (clearance della creatinina ≤50 ml/min) vedere il paragrafo 4.4 e il paragrafo 5.2.
I pazienti con compromissione epatica possono utilizzare tiotropio bromuro alla dose raccomandata (vedere paragrafo 5.2).
Popolazione pediatrica
Tiotropio Teva Italia non deve essere usato nei bambini e negli adolescenti di età inferiore ai 18 anni. Non sono state determinate la sicurezza e l'efficacia. Non ci sono dati disponibili.
Non si riscontra un uso significativo di tiotropio bromuro nella popolazione pediatrica per l'indicazione di BPCO.
La sicurezza e l'efficacia di tiotropio bromuro per la fibrosi cistica nei bambini e negli adolescenti di età inferiore a 18 anni non sono state stabilite. Non ci sono dati disponibili.
Modo di somministrazione/Istruzioni per la manipolazione e l'uso
Per garantire una corretta somministrazione del medicinale, il paziente deve essere istruito sull'utilizzo dell'inalatore da parte del medico o di un altro operatore sanitario.
L'inalatore Zonda è stato messo a punto appositamente per le capsule di Tiotropio Teva Italia. I pazienti non devono utilizzarlo per l'assunzione di altri medicinali. Le capsule di Tiotropio Teva Italia devono essere inalate esclusivamente utilizzando l'inalatore Zonda. I pazienti non devono utilizzare altri inalatori per assumere le capsule di Tiotropio Teva Italia. Raccomandare al paziente di seguire attentamente le istruzioni per l'uso riportate nel foglio illustrativo. Informare il paziente delle immagini supplementari all'interno del coperchio della scatola che mostrano il metodo corretto per l'inserimento della capsula nell'inalatore. Per evitare il rischio di soffocamento, informare il paziente di non inserire MAI una capsula direttamente nel boccaglio.
L'inalatore Zonda deve essere utilizzato soltanto con il flacone di capsule che viene fornito nella stessa confezione dell'inalatore o in una confezione impacchettata separatamente a quella dell'inalatore. Non riutilizzare l'inalatore per un altro flacone di capsule. Gettare il dispositivo Zonda dopo 30 utilizzi (15 utilizzi se utilizzato con la confezione da 15 capsule).
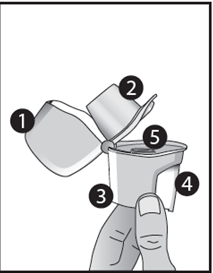
- Cappuccio di chiusura antipolvere
- Boccaglio
- Base
- Pulsante di foratura
- Camera centrale
1. Sollevare il cappuccio di chiusura antipolvere
- Afferrando saldamente la base dell'inalatore, aprire il boccaglio spingendolo verso l'alto, nella direzione indicata dalla freccia
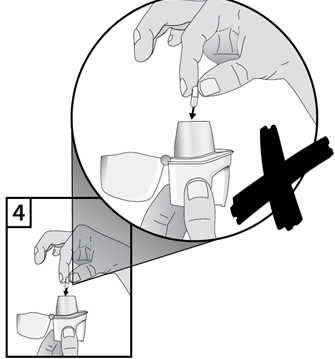
- Estrarre una capsula di Tiotropio Teva Italia dal flacone immediatamente prima dell'uso e chiudere bene il flacone. Inserire una capsula nell'apposita camera centrale nella base dell'inalatore. Non conservare la capsula nell'inalatore Zonda.
- Per evitare il rischio di soffocamento, non inserire MAI una capsula direttamente nel boccaglio
- Chiudere il boccaglio fino a quando si sente un clic, lasciando aperto il cappuccio di chiusura antipolvere
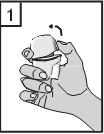
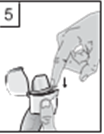
- Tenendo l'inalatore con il boccaglio rivolto verso l'alto, premere a fondo una volta il pulsante di foratura e rilasciarlo. Questa azione fora la capsula permettendo il rilascio del farmaco durante l'inspirazione.
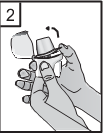
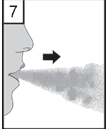
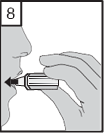
- Espirare completamente mantenendosi a distanza dal boccaglio. Evitare sempre di respirare nel boccaglio.
- Portare il boccaglio alla bocca e tenere la testa in posizione verticale. Chiudere le labbra intorno al boccaglio e inspirare lentamente e profondamente ma a una velocità sufficiente a udire o sentire vibrare la capsula dentro la camera centrale. Trattenere il respiro fino a quando possibile e nello stesso tempo sfilare l'inalatore dalla bocca. Riprendere a respirare normalmente. Ripetere i punti 7 e 8 per svuotare completamente la capsula.
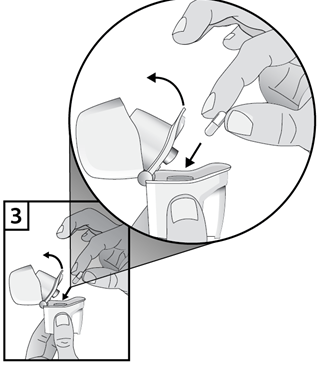
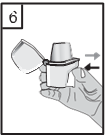
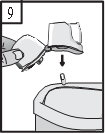
- Dopo l'uso, aprire nuovamente il boccaglio, rovesciare la capsula vuota ed estrarla. Chiudere il boccaglio e il cappuccio di chiusura antipolvere e riporre l'inalatore Zonda.
Le capsule di Tiotropio Teva Italia contengono solo una piccola quantità di polvere, quindi la capsula è riempita solo in parte.
Se necessario, dopo l'uso è possibile pulire il boccaglio dell'inalatore Zonda con un panno asciutto o un fazzolettino.
Controindicazioni
Quando non dev'essere usato Tiotropio Teva Italia
Ipersensibilità al principio attivo Tiotropio Bromuro, all'atropina o ai suoi derivati, per esempio ipratropio o ossitropio, o ad uno qualsiasi degli eccipienti elencati al paragrafo 6.1, compreso il lattosio monoidrato che contiene proteine del latte.
Avvertenze speciali e precauzioni di impiego
Cosa serve sapere prima di prendere Tiotropio Teva Italia
Tiotropio Bromuro, essendo un broncodilatatore di mantenimento da assumere una volta al giorno, non deve essere utilizzato nel trattamento iniziale di episodi acuti di broncospasmo, cioè come terapia di emergenza.
Possono verificarsi reazioni di ipersensibilità immediata dopo la somministrazione di tiotropio bromuro polvere per inalazione.
In linea con la sua attività anticolinergica, tiotropio bromuro deve essere utilizzato con cautela nei pazienti con glaucoma ad angolo chiuso, iperplasia prostatica od ostruzione del collo della vescica (vedere paragrafo 4.8).
Come nel caso di altre terapie inalatorie, il medicinale può causare broncospasmo paradosso con un aumento immediato di sibilo e dispnea dopo la somministrazione. Il broncospasmo paradosso risponde ad un broncodilatatore ad azione rapida e deve essere trattato immediatamente. Tiotropio Teva Italia deve essere interrotto immediatamente, il paziente deve essere visitato e, se necessario, deve essere istituita una terapia alternativa.
Tiotropio deve essere utilizzato con cautela nei pazienti con infarto miocardico recente, verificatosi da meno di 6 mesi; nei pazienti che abbiano manifestato una qualsiasi aritmia instabile o pericolosa per la vita, o un'aritmia cardiaca che abbia richiesto un intervento o una modifica della terapia farmacologica nell'anno precedente; nei pazienti ospedalizzati per insufficienza cardiaca (Classe NYHA III o IV) nell'anno precedente. Tali pazienti sono stati esclusi dagli studi clinici, e queste condizioni possono essere influenzate dal meccanismo d'azione anticolinergico.
Poiché la concentrazione plasmatica del medicinale aumenta al diminuire della funzionalità renale, nei pazienti con danno renale da moderato a grave (clearance della creatinina ≤ 50 ml/min) tiotropio bromuro deve essere utilizzato solo se i benefici attesi superano i potenziali rischi. Non ci sono dati a lungo termine in pazienti con danno renale grave (vedere paragrafo 5.2).
I pazienti devono essere avvisati di evitare che la polvere del medicinale venga a contatto con gli occhi. Devono essere informati che ciò può avere come conseguenza una precipitazione o un peggioramento del glaucoma ad angolo chiuso, dolore o disturbo oculare, temporaneo offuscamento della vista, aloni visivi o immagini colorate in associazione ad occhi arrossati da congestione congiuntivale ed edema corneale. Se si dovesse sviluppare una qualsiasi combinazione di questi sintomi oculari, i pazienti devono sospendere l'utilizzo di tiotropio bromuro e consultare immediatamente uno specialista.
La secchezza della bocca che è stata osservata con il trattamento con anticolinergici, nel lungo termine può essere associata a carie dentarie.
Tiotropio bromuro non deve essere utilizzato più di una volta al giorno (vedere paragrafo 4.9).
Ogni capsula contiene 18 mg di lattosio monoidrato. I pazienti con rari problemi ereditari di intolleranza al galattosio, deficit di Lapp lattasi o malassorbimento di glucosio-galattosio non devono assumere questo medicinale. L'eccipiente lattosio può contenere tracce di proteine del latte, le quali possono causare reazioni allergiche nei pazienti con grave ipersensibilità o allergia alle proteine del latte.
Interazioni con altri medicinali e altre forme di interazione
Quali farmaci o alimenti possono modificare l'effetto di Tiotropio Teva Italia
Benché non siano stati effettuati studi formali di interazione farmacologica, tiotropio bromuro polvere per inalazione è stato utilizzato in concomitanza con altri medicinali senza evidenza clinica di interazioni. Questi comprendono broncodilatatori simpaticomimetici, metilxantine, steroidi orali e per inalazione, comunemente utilizzati nel trattamento della BPCO.
Non è emerso che l'uso di β2-agonisti a lunga durata (LABA) o corticosteroidi inalatori (ICS) alteri l'esposizione a tiotropio.
La co-somministrazione di tiotropio bromuro ed altri medicinali contenenti anticolinergici non è stata studiata e pertanto non è raccomandata.
Fertilità, gravidanza e allattamento
Fertilità
Per tiotropio non sono disponibili dati clinici relativi alla fertilità. Uno studio non clinico eseguito con tiotropio non ha messo in evidenza alcun effetto avverso sulla fertilità (vedere paragrafo 5.3).
Gravidanza
I dati relativi all'uso di tiotropio in donne in gravidanza sono molto limitati. Gli studi sugli animali non indicano effetti dannosi diretti o indiretti con riferimento alla tossicità riproduttiva a dosi clinicamente rilevanti (vedere paragrafo 5.3). A scopo precauzionale, è preferibile evitare l'uso di Tiotropio Teva Italia durante la gravidanza.
Allattamento
Non è noto se Tiotropio Bromuro sia escreto nel latte materno. Nonostante studi effettuati su roditori abbiano dimostrato che solo una piccola quantità di tiotropio bromuro è escreta nel latte materno, l'uso di tiotropio bromuro non è raccomandato durante l'allattamento. Tiotropio bromuro è una sostanza a lunga durata d'azione. La decisione di continuare o sospendere l'allattamento piuttosto che continuare o sospendere la terapia con Tiotropio Teva Italia deve essere presa tenendo in considerazione il beneficio dell'allattamento per il bambino e il beneficio della terapia con Tiotropio Teva Italia per la madre.
Effetti sulla capacità di guidare veicoli e sull'uso di macchinari
Non sono stati effettuati studi relativi agli effetti sulla capacità di guidare veicoli e di usare macchinari. Il verificarsi di capogiri, visione offuscata o cefalea può influire sulla capacità di guidare veicoli e sull'uso di macchinari.
Effetti indesiderati
Quali sono gli effetti collaterali di Tiotropio Teva Italia
Molti degli effetti indesiderati elencati possono essere attribuiti alle proprietà anticolinergiche di Tiotropio Bromuro.
La frequenza assegnata agli effetti indesiderati sotto elencati è basata sui tassi grezzi di incidenza delle reazioni avverse al medicinale (cioè eventi attribuiti a tiotropio) osservati nel gruppo trattato con tiotropio (9.647 pazienti), ottenuti raggruppando i dati derivanti da 28 studi clinici controllati verso placebo che prevedevano periodi di trattamento compresi tra quattro settimane e quattro anni.
Le frequenze sono state definite utilizzando la convenzione seguente:
Molto comune (≥1/10); comune (da ≥1/100 a <1/10); non comune (da ≥1/1000 a <1/100); raro (da ≥1/10.000 a <1/1000); molto raro (<1/10.000), non nota (la frequenza non può essere definita sulla base dei dati disponibili).
|
Classificazione per sistemi e organi secondo MedDRA
|
Frequenza
|
|
Disturbi del metabolismo e della nutrizione
|
|
|
Disidratazione
|
Non nota
|
|
Patologie del sistema nervoso
|
|
| Capogiro | Non comune |
| Cefalea | Non comune |
| Alterazioni del gusto | Non comune |
|
Insonnia
|
Raro
|
|
Patologie dell'occhio
|
|
| Visione offuscata | Non comune |
| Glaucoma | Raro |
|
Pressione intraoculare aumentata
|
Raro
|
|
Patologie cardiache
|
|
| Fibrillazione atriale | Non comune |
| Tachicardia sopraventricolare |
Raro
|
| Tachicardia |
Raro
|
|
Palpitazioni
|
Raro
|
|
Patologie respiratorie, toraciche e mediastiniche
|
|
|
Faringite
|
Non comune |
| Disfonia | Non comune |
|
Tosse
|
Non comune |
| Broncospasmo | Raro |
| Epistassi | Raro |
| Laringite | Raro |
|
Sinusite
|
Raro
|
|
Patologie gastrointestinali
|
|
| Bocca secca | Comune |
| Malattia da reflusso gastroesofageo | Non comune |
| Stipsi | Non comune |
| Candidiasi orofaringea | Non comune |
| Ostruzione intestinale, incluso ileo paralitico | Raro |
| Gengivite | Raro |
| Glossite | Raro |
| Disfagia | Raro |
| Stomatite | Raro |
| Nausea | Raro |
|
Carie dentarie
|
Non nota
|
|
Patologie della cute e del tessuto sottocutaneo, disturbi del sistema immunitario
|
|
| Eruzione cutanea | Non comune |
| Orticaria | Raro |
| Prurito | Raro |
|
Ipersensibilità (comprese reazioni immediate)
|
Raro |
| Angioedema | Raro |
| Reazione anafilattica |
Non nota
|
| Infezione della cute, ulcera della cute |
Non nota
|
|
Cute secca
|
Non nota
|
|
Patologie del sistema muscoloscheletrico e del tessuto connettivo
|
|
|
Tumefazione articolare
|
Non nota
|
|
Patologie renali e urinarie
|
|
| Disuria | Non comune |
| Ritenzione di urina | Non comune |
|
Infezione delle vie urinarie
|
Raro
|
Reazioni allergiche
L'eccipiente lattosio può contenere tracce di proteine del latte, le quali possono causare reazioni allergiche nei pazienti con grave ipersensibilità o allergia alle proteine del latte.
Tiotropio bromuro deve essere immediatamente interrotto se si verifica una reazione da ipersensibilità o una reazione allergica, e il paziente deve poi essere gestito nella maniera consueta.
Broncospasmo paradosso
Come nel caso di altre terapie inalatorie, il medicinale può causare broncospasmo paradosso, con un aumento immediato di sibilo e dispnea dopo la somministrazione. Il broncospasmo paradosso risponde ad un broncodilatatore ad azione rapida e deve essere trattato immediatamente. Tiotropio Teva Italia deve essere interrotto immediatamente, il paziente deve essere visitato e, se necessario, deve essere istituita una terapia alternativa.
Descrizione di reazioni avverse selezionate
Negli studi clinici controllati, gli effetti indesiderati comunemente osservati erano quelli anticolinergici, come la bocca secca che si è verificata in circa il 4% dei pazienti.
In 28 studi clinici, la bocca secca ha portato all'interruzione del trattamento in 18 dei 9.647 pazienti trattati con tiotropio (0,2%).
Effetti indesiderati gravi coerenti con gli effetti anticolinergici includono glaucoma, stipsi ed ostruzione intestinale (compreso ileo paralitico), così come la ritenzione di urina.
Altre popolazioni speciali
Un aumento dell'incidenza degli effetti anticolinergici può verificarsi con l'aumentare dell'età.
Segnalazione delle reazioni avverse sospette
La segnalazione delle reazioni avverse sospette che si verificano dopo l'autorizzazione del medicinale è importante in quanto permette un monitoraggio continuo del rapporto beneficio/rischio del medicinale. Agli operatori sanitari è richiesto di segnalare qualsiasi reazione avversa sospetta tramite il sistema nazionale di segnalazione all'indirizzo www.agenziafarmaco.gov.it/content/come-segnalare-una-sospetta-reazione-avversa
Sovradosaggio
Cosa fare se avete preso una dose eccessiva di Tiotropio Teva Italia
Dosi elevate di Tiotropio Bromuro possono indurre la comparsa di segni e sintomi anticolinergici.
Comunque, nei volontari sani non sono stati osservati effetti avversi sistemici anticolinergici a seguito dell'inalazione di una dose unica fino a 340 microgrammi di tiotropio bromuro. Inoltre, non sono stati osservati effetti avversi rilevanti, oltre alla secchezza della bocca, a seguito della somministrazione in volontari sani di tiotropio bromuro fino a 170 microgrammi per 7 giorni. In uno studio a dosi multiple condotto in pazienti con BPCO trattati con una dose massima giornaliera di 43 microgrammi di tiotropio bromuro per 4 settimane non sono stati osservati effetti indesiderati significativi.
Tiotropio bromuro è caratterizzato da una bassa biodisponibilità orale, pertanto è improbabile che l'ingestione involontaria delle capsule per via orale possa causare un'intossicazione acuta.
Scadenza
24 mesi
Dopo la prima apertura: 30 giorni (flacone da 15 capsule) o 60 giorni (flacone da 30 capsule)
Conservazione
Tenere il flacone ben chiuso. Conservare nella confezione originale per proteggere il medicinale dall'umidità.
Non refrigerare o congelare.
Farmaci Equivalenti
I farmaci equivalenti di
Tiotropio Teva Italia a base di
Tiotropio Bromuro sono:
Sirkava, Spiriva, Tiotropio Doc
Foglietto Illustrativo
Fonti Ufficiali
© 2022 EDRA S.p.A. - P.iva 08056040960
DPO - dpo@lswr.it