Vitaros
Ultimo aggiornamento: 09/01/2024
Cos'è Vitaros?
Vitaros è un farmaco a base del principio attivo
Alprostadil, appartenente alla categoria degli
Disfunzione erettile e nello specifico
Farmaci usati nella disfunzione dell'erezione. E' commercializzato in Italia dall'azienda
The Simple Pharma Company Limited.
Vitaros può essere prescritto con Ricetta RR - medicinali soggetti a prescrizione medica.
Vitaros può essere prescritto con Ricetta RR - medicinali soggetti a prescrizione medica.
Confezioni
Vitaros 3 mg/g crema 4 contenitori monodose da 100 mg
Informazioni commerciali sulla prescrizione
Titolare: The Simple Pharma Company Limited
Ricetta: RR - medicinali soggetti a prescrizione medica
Classe: C
Principio attivo: Alprostadil
Gruppo terapeutico: Disfunzione erettile
ATC: G04BE01 - Alprostadil
Forma farmaceutica: crema
Ricetta: RR - medicinali soggetti a prescrizione medica
Classe: C
Principio attivo: Alprostadil
Gruppo terapeutico: Disfunzione erettile
ATC: G04BE01 - Alprostadil
Forma farmaceutica: crema
Se sei un professionista, potrai trovare le schede tecniche complete e molto altro nell'area riservata di Codifa.it
Indicazioni
Perché si usa Vitaros? A cosa serve?
Trattamento della disfunzione erettile nell'uomo di età ≥ 18 anni. La disfunzione erettile è l'incapacità di raggiungere o mantenere un'erezione sufficiente per permettere un rapporto sessuale soddisfacente.
Posologia
Come usare Vitaros: Posologia
Vitaros viene applicato sulla punta del pene.
Vitaros deve essere utilizzato in quantità necessaria per raggiungere l'erezione. Ogni contenitore AccuDose di Vitaros è solo monouso e deve essere correttamente smaltito dopo l'uso. L'effetto compare 5-30 minuti dopo la somministrazione. La durata dell'effetto è di circa 1- 2 ore. Tuttavia, la durata effettiva varia da paziente a paziente. Ogni paziente deve essere istruito da un medico esperto sulla tecnica adeguata per la somministrazione di Vitaros prima di procedere con l'autosomministrazione. La frequenza massima di somministrazione è di non più di 2-3 volte nell'arco di una settimana e solo una volta in un periodo di 24 ore.
La dose iniziale deve essere raccomandata da un medico. Una dose iniziale di 300 mcg può essere considerata specialmente nei pazienti con grave disfunzione erettile, co-morbidità o mancanza di risposta agli inibitori della PDE-5. I pazienti che non tollerano la dose da 300 mcg a causa di effetti indesiderati locali possono scendere alla dose inferiore di 200 mcg.
Ai pazienti devono essere fornite istruzioni sulla tecnica corretta di somministrazione, sui possibili effetti indesiderati (per esempio capogiri, svenimento) e la necessità di evitare l'uso di macchinari fino a quando non risulti chiaro il livello di tolleranza individuale del farmaco. Nello studio clinico è stata rilevata una frequenza di abbandono superiore nel gruppo trattato con 300 mcg rispetto al gruppo 200 mcg, rispettivamente del 30% e 20%.
Modo di somministrazione
Si raccomanda di urinare prima di applicare il farmaco. Dopo aver rimosso il cappuccio, applicare tutto il contenuto di Vitaros nell'apertura alla punta del pene (meato) circa 5-30 minuti prima di iniziare il rapporto sessuale seguendo le istruzioni riportate di seguito.
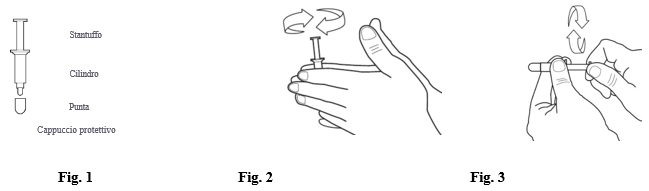
- Lavarsi le mani prima di applicare Vitaros. Rimuovere il contenitore AccuDose dalla bustina strappando completamente il sigillo dalla metà del bordo superiore.
Rimuovere il contenitore AccuDose (vedere Fig. 1) dalla bustina. Conservare la bustina per eliminare successivamente il contenitore AccuDose usato. - Portare il contenuto del contenitore monodose a temperatura ambiente strofinandolo tra le mani (vedi Fig. 2). Questa operazione può essere evitata se la bustina è stata rimossa in precedenza dal frigorifero (entro il periodo indicato nel paragrafo 6.4 Precauzioni particolari per la conservazione) e il contenuto ha già raggiunto la temperatura ambiente.
- Ruotare più volte lo stantuffo per assicurarsi che possa scivolare facilmente (vedere Fig. 3).
Quindi rimuovere il cappuccio dalla punta del contenitore AccuDose.
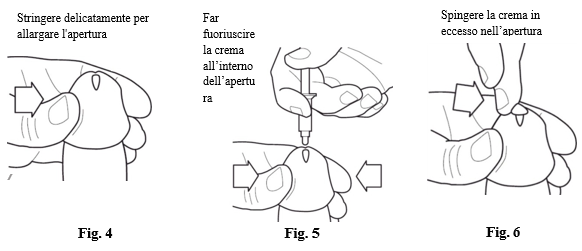
- Afferrare la punta del pene con una mano e stringerla delicatamente per allargare l'apertura alla punta del pene, tenendolo in una posizione verticale (vedi Fig. 4) (nota, se non è circonciso, abbassi prima il prepuzio e lo trattenga in tale posizione mentre successivamente allarga l'apertura alla punta del pene).
- Tenere il cilindro del contenitore AccuDose tra le dita e senza inserirlo nel pene (vedere Fig. 5), posizionare la punta del contenitore il più possibile vicino all'apertura alla punta del pene in modo che la crema scenda nell'uretra. Ricordarsi di spingere tutta la crema dal contenitore AccuDose. Lentamente, ma fermamente, spingere verso il basso lo stantuffo con il pollice o il dito fino a quando tutta la crema non viene espulsa nell'apertura alla punta del pene e lungo l'uretra.
Nota: siccome è importante che tutta la crema scenda nell'uretra, fare attenzione a non inserire la punta del contenitore AccuDose nell'apertura alla punta del pene. - Tenere il pene in posizione verticale per circa 30 secondi per permettere alla crema di penetrare. Ci sarà probabilmente della crema che inizialmente non si inserisce nell'apertura alla punta del pene. Tutta la quantità di crema in eccesso che copre l'apertura alla punta del pene deve essere spinta nell'apertura con la punta di un dito (vedi Fig. 6). Non utilizzare un secondo contenitore AccuDose per compensare la crema non introdotta nell'apertura alla punta del pene. Non urinare immediatamente dopo l'applicazione, il farmaco potrebbe uscire prima che l'effetto abbia inizio.
- Ricordi che ogni dose di Vitaros è solo per una singola somministrazione. Rimettere il cappuccio sulla punta del contenitore AccuDose e riporlo nella bustina aperta, piegare e smaltire in conformità alla normativa locale vigente.
- Vitaros può essere irritante per gli occhi. Lavarsi le mani dopo l'applicazione di Vitaros.
Controindicazioni
Quando non dev'essere usato Vitaros
Vitaros non deve essere usato in pazienti con una qualsiasi delle seguenti condizioni:
- Affetti da patologie pregresse quali ipotensione ortostatica, infarto del miocardio e sincope.
- Affetti da ipersensibilità nota ad Alprostadil o ad uno degli eccipienti di Vitaros.
- Affetti da condizioni che potrebbero predisporre al priapismo, quali anemia falciforme o a tratto falciforme, trombocitemia, policitemia o mieloma multiplo, o leucemia.
- Con anatomia anomala del pene, quali ipospadia grave, nei pazienti con deformazioni anatomiche del pene, come un'anormale curvatura, e nei pazienti con uretrite e balanite (infiammazione/infezione del glande del pene).
- Inclini a trombosi venosa o che hanno una sindrome da iperviscosità e quindi sono ad aumentato rischio di priapismo (erezione rigida della durata di 4 o più ore).
- Per i quali l'attività sessuale è sconsigliata come negli uomini con condizioni cardiovascolari o cerebrovascolari instabili.
- Vitaros non deve essere utilizzato per un rapporto sessuale con una donna in età fertile a meno che la coppia non utilizzi un preservativo.
Avvertenze speciali e precauzioni di impiego
Cosa serve sapere prima di prendere Vitaros
Effetti locali
Erezioni prolungate della durata > 4 ore (priapismo), anche se rare, sono state osservate con l'uso di Vitaros.
Il priapismo è stato osservato in due studi a 3 mesi in 1 paziente (0,06%) e nello studio > 6 mesi in 5 (0,4%) pazienti, di cui 4 (0,3%) nel gruppo da 200 mcg e 1 (0,1%) nel gruppo da 300 mcg. In caso di priapismo, il paziente deve essere informato di cercare immediata assistenza medica. Se il priapismo non viene trattato immediatamente, può causare un danno al tessuto del pene e una perdita permanente di potenza.
Ipotensione sintomatica (capogiri) e sincope si sono verificati in una piccola percentuale di pazienti (2/459 (0,4%), 6/1591 (0,4%), e 6/1280 (0,5%) a dosi di Alprostadil di 100, 200 e 300 mcg, rispettivamente, durante gli studi di Fase 3. I pazienti devono essere avvertiti di evitare attività, come guidare o eseguire attività pericolose, che potrebbero provocare incidenti nel caso insorgesse sincope in seguito alla somministrazione di Vitaros.
Prima di iniziare il trattamento con Vitaros, le cause di disfunzione erettile, che sono trattabili, devono essere escluse mediante appropriati metodi diagnostici.
Inoltre, i pazienti con patologie pregresse, come ipotensione ortostatica, infarto del miocardio e sincope, non devono utilizzare Vitaros (vedi CONTROINDICAZIONI, paragrafo 4.3).
Non sono stati condotti studi clinici in pazienti con una storia di patologia neurologica o lesione spinale.
La farmacocinetica di Vitaros non è stata valutata in pazienti con insufficienza epatica e/o renale. Potrebbe essere necessario ridurre il dosaggio in queste popolazioni a causa di compromissione del metabolismo.
Precauzioni generali
Vitaros deve essere applicato seguendo le istruzioni riportate sopra. L'esposizione intrauretrale involontaria può causare bruciore al pene o sensazione di formicolio e dolore. L'effetto della esposizione ripetuta a lungo termine intrauretrale di Vitaros è sconosciuto.
I pazienti devono essere informati che Vitaros non offre alcuna protezione alla diffusione di malattie sessualmente trasmissibili. I pazienti e le partner che utilizzano Vitaros devono essere consigliati circa le misure di protezione necessarie per evitare la diffusione di agenti trasmissibili sessualmente, compreso il virus dell'immunodeficienza umana (HIV). Gli operatori sanitari devono incoraggiare i loro pazienti a informare le loro partner sessuali che stanno utilizzando Vitaros. Le partner di coloro che utilizzano Vitaros possono manifestare eventi avversi, più comunemente irritazione vaginale. Si raccomanda pertanto l'uso di un preservativo.
Non sono stati studiati gli effetti di Vitaros sulla mucosa orale o anale. Un preservativo deve essere usato in caso di sesso orale (fellatio) o sesso anale.
Vitaros non ha proprietà contraccettive. Si raccomanda che le coppie che utilizzano Vitaros usino una contraccezione adeguata se la partner è in età fertile.
Non ci sono informazioni sugli effetti durante la prima fase di gravidanza di alprostadil relativamente alle quantità ricevute dalle partner di sesso femminile. Deve essere utilizzato un preservativo in caso di rapporti sessuali con donne in età fertile, donne in gravidanza o che allattano.
L'utilizzo del farmaco è stato studiato solo unitamente a preservativi a base di lattice, non si possono escludere eventuali rischi di danni a preservativi composti da altri materiali.
Questo medicinale contiene 5 mg di alcol (etanolo) per ogni dose da 100 mg, pari a 50 mg/g (5% p/p). Può causare una sensazione di bruciore sulla pelle danneggiata.
Interazioni con altri medicinali e altre forme di interazione
Quali farmaci o alimenti possono modificare l'effetto di Vitaros
Non sono stati condotti studi di interazione di farmacocinetica o farmacodinamica con Vitaros. Basandosi sul metabolismo del farmaco (vedere “Proprietà farmacocinetiche”), interazioni farmaco-farmaco sono da considerarsi improbabili.
Effetti di interazione
Non è stata studiata la sicurezza e l'efficacia di Vitaros, in concomitanza con altri trattamenti per la disfunzione erettile, in particolare con gli inibitori della fosfodiesterasi-5 (PDE-5) o sildenafil, tadalafil e vardenafil. Pertanto, Vitaros non deve essere usato in associazione con gli inibitori della PDE5. Poiché sia Vitaros sia gli inibitori della PDE5 hanno effetti cardiovascolari, un ulteriore aumento del rischio cardiovascolare non può essere escluso.
Non sono stati effettuati studi di interazione relativi all'impiego di Vitaros in pazienti con impianto penieno o trattati con rilassanti della muscolatura liscia come la papaverina e farmaci usati per indurre l'erezione come i farmaci alfa bloccanti (ad esempio fentolamina intracavernosa, timoxamina). C'è un rischio di priapismo (erezione anomala prolungata dolorosa) se Vitaros viene usato in concomitanza con questi farmaci.
Non sono stati effettuati studi di interazione tra Vitaros e simpaticomimetici, decongestionanti e soppressori dell'appetito. Quando usato in associazione con questi medicinali Vitaros può avere un effetto ridotto (inibizione dell'effetto farmacologico).
Non sono stati effettuati studi di interazione tra Vitaros e farmaci anticoagulanti o inibitori dell'aggregazione piastrinica. L'uso di Vitaros in associazione con tali farmaci potrebbe aumentare il rischio di sanguinamento uretrale ed ematuria.
L'associazione con farmaci antipertensivi e farmaci vasoattivi potrebbe aumentare il rischio di ipotensione; soprattutto negli anziani.
Fertilità, gravidanza e allattamento
Gravidanza
Non vi sono dati riguardanti l'uso di Vitaros in donne in gravidanza. L'esposizione indiretta all'Alprostadil nelle donne è probabilmente bassa.
I dati sugli animali dopo esposizione a dosi elevate di alprostadil mostrano effetti tossici sulla riproduzione (vedere paragrafo 5.3).
Le donne in gravidanza non devono essere esposte a Vitaros.
Allattamento
Non è noto se l'esposizione indiretta all'alprostadil porti ad una significativa escrezione nel latte materno. Non è raccomandato l'uso di Vitaros durante l'allattamento.
Fertilità
In conigli maschi, è stata osservata atrofia dei tubuli seminiferi dei testicoli dopo somministrazione ripetuta. Non è noto se Vitaros ha un effetto sulla fertilità maschile umana.
Effetti sulla capacità di guidare veicoli e sull'uso di macchinari
Non sono stati effettuati studi sugli effetti sulla capacità di guidare veicoli e sull'uso di macchinari.
Poiché capogiri e sincope (svenimento), sono stati riportati raramente durante gli studi clinici con Vitaros, i pazienti devono evitare mansioni, come la guida o attività rischiose, per almeno 1-2 ore dopo la somministrazione di Vitaros, in quanto l'insorgenza di sincope potrebbe provocare incidenti.
Effetti indesiderati
Quali sono gli effetti collaterali di Vitaros
Tabella delle reazioni avverse
Gli eventi avversi più frequentemente riportati in trattamento con Vitaros sono elencati nella tabella sottostante (molto comune ≥ 1/10; comune ≥ 1/100, <1/10, non comune ≥ 1/1000, <1/100, raro ≥ 1/10000, <1/1000, molto raro <1/10000).
Il priapismo (una erezione che dura più di 4 ore) è una condizione grave che richiede un trattamento immediato da parte di un medico.
Tabella 1. Reazioni Avverse
|
Classificazione sistemica organica (MedDRA)
|
Frequenza
|
Reazioni avverse
|
|
Patologie del sistema nervoso
|
Non comune
|
Iperestesia
|
|
Patologie vascolari*
|
Non comune
|
Capogiri
Sincope
Ipotensione
|
|
Patologie della cute e del tessuto
|
Comune
|
Eruzione cutanea
|
|
Patologie del tessuto muscoloscheletrico
|
Non comune
|
Dolore alle estremità
|
|
Patologie renali e urinarie
|
Comune
|
Dolore uretrale
|
|
Non comune
|
Stenosi uretrale Infiammazione delle vie urinarie
|
|
|
Patologie dell'apparato riproduttivo e della mammella
|
Comune
|
Bruciore al pene
Dolore al pene
Eritema al pene
Dolore genitale
Eritema al pene
Disturbo genitale
Eritema genitale
Aumento dell'erezione
Prurito ai genitali
Edema del pene
Balanite
Formicolio del pene
Pulsazioni del pene
Intorpidimento del peneNelle donne partner: Sensazione di bruciore vulvovaginale Vaginite |
|
Non comune
|
Prurito del pene Nelle donne partner: |
|
|
Patologie sistemiche e condizioni relative alla sede di somministrazione
|
Non comune
|
Dolore alla sede di somministrazione
|
Popolazioni speciali
*Non vi è alcuna chiara indicazione che Alprostadil causi un aumento del rischio di eventi cardiovascolari, ad eccezione degli effetti vasodilatatori. Tuttavia, non si può escludere che i pazienti con pregressa malattia o fattori di rischio abbiano un rischio aumentato di avere eventi, in concomitanza con un aumento dell'attività sessuale/fisica che è associata all'uso di alprostadil (vedere paragrafi 4.3 e 4.4).
Segnalazione delle reazioni avverse sospette
La segnalazione delle reazioni avverse sospette che si verificano dopo l'autorizzazione del medicinale è importante, in quanto permette un monitoraggio continuo del rapporto beneficio/rischio del medicinale. Agli operatori sanitari è richiesto di segnalare qualsiasi reazione avversa sospetta tramite www.agenziafarmaco.gov.it/content/come-segnalare-una-sospetta-reazione-avversa.
Sovradosaggio
Cosa fare se avete preso una dose eccessiva di Vitaros
Con Vitaros non sono stati riportati casi di sovradosaggio che richiedevano un trattamento. In caso di sovradosaggio con Vitaros, si potrebbe verificare ipotensione, sincope, capogiri, dolore penieno e possibile priapismo (erezione rigida che dura per più di 4 ore). Il priapismo può causare peggioramento permanente della funzione erettile. I pazienti con sospetto di sovradosaggio che manifestano questi sintomi devono essere tenuti sotto stretta sorveglianza medica fino a che i sintomi locali o sistemici non siano risolti.
Si deve informare il paziente di consultare immediatamente un medico, se l'erezione perdura per più di 4 ore.
Devono essere presi i seguenti provvedimenti:
- far stendere il paziente supino o sul fianco. Applicare alternativamente per due minuti su ciascun lato superiore interno della coscia del ghiaccio (questo dovrebbe portare ad un rilasciamento riflesso delle valvole venose). Se non si ottiene risposta entro 10 minuti, interrompere il trattamento.
- Se questo trattamento è inefficace e l'erezione perdura per più di 6 ore, si deve effettuare un'aspirazione peniena. Usando procedure sterili, inserire un ago butterfly di calibro 19-21 nel corpo cavernoso e aspirare 20-50 ml di sangue. Questo dovrebbe portare a una detumescenza del pene. Se necessario, ripetere l'operazione sul lato opposto del pene.
- Se il trattamento non ha successo, si raccomanda la somministrazione di un farmaco α- adrenergico per iniezione intercavernosa. Questa operazione deve essere effettuata con cautela, anche se nel trattamento del priapismo l'abituale controindicazione alla somministrazione intrapeniena di un vasocostrittore non è valida. Si devono monitorare continuamente la pressione arteriosa e la frequenza cardiaca durante la procedura. Estrema cautela va usata in pazienti che presentano patologie delle coronarie, ipertensione non controllata, ischemia cerebrale, e in tutti i soggetti che sono in trattamento con inibitori delle MAO (mono ammino ossidasi). In quest'ultimo caso, devono essere disponibili i presidi per il controllo delle crisi ipertensive.
- Si deve preparare una soluzione di 200 microgrammi/ml di fenilefrina e iniettare, ogni 5-10 minuti, da 0,5 a 1,0 ml di soluzione. In alternativa può essere usata una soluzione di 20 microgrammi/ml di adrenalina. Se necessario, questo può essere seguito da una ulteriore aspirazione di sangue tramite lo stesso ago butterfly. La massima dose di fenilefrina deve essere di 1 mg, quella di adrenalina 100 microgrammi (5 ml di soluzione).
- Come alternativa può essere usato metaraminolo, ma si deve tener presente che sono state riportate crisi ipertensive fatali dopo la somministrazione di questo farmaco. Se anche questo trattamento si dimostra inefficace a risolvere il priapismo, il paziente deve essere immediatamente sottoposto a trattamento chirurgico.
Scadenza
1 anno
Una volta aperto, usare immediatamente, eliminare qualsiasi parte inutilizzata.
Conservazione
Conservare in frigorifero (2°C - 8°C).
Non congelare.
Le bustine sigillate possono essere conservate fuori dal frigorifero da parte del paziente, ad una temperatura inferiore a 25°C fino a un massimo di 3 giorni prima dell'utilizzo.
Al termine di questo periodo, il prodotto deve essere eliminato.
Conservare nella confezione originale per proteggere il medicinale dalla luce.
Foglietto Illustrativo
Fonti Ufficiali
© 2022 EDRA S.p.A. - P.iva 08056040960
DPO - dpo@lswr.it